生理学与病理生理学系郑铭课题组《Circulation Research》发文揭示心肌细胞线粒体间通讯的分子机制
2019年8月28日,北京大学基础医学院生理学与病理生理学系郑铭课题组在《Circulation Research》在线发表题为:“Miro2 Regulates Inter-Mitochondrial Communication in the Heart and Protects Against TAC-Induced Cardiac Dysfunction”的研究论文。文章首次报道了线粒体蛋白Miro2调控心肌细胞线粒体间交互作用的分子机制及其在心肌肥厚过程中的病理生理学意义。
哺乳动物成年心肌细胞大约含6000个线粒体,呈“晶格状”排列在肌原纤维间,线粒体运动及线粒体间融合-分裂活动受限。郑铭课题组前期研究发现,成年心肌细胞线粒体之间通过kissing(吻合)和nanotunneling (纳米通道)两种方式交互作用,从而在整个心肌细胞内形成一个连续的动态功能网络(PNAS, 2013)。但调控线粒体间通讯的分子机制及其病理生理学意义仍不清楚。
本研究使用线粒体定位的光激活绿色荧光蛋白mtPAGFP,结合活细胞实时荧光成像,发现线粒体间纳米通道多与细胞骨架蛋白微管伴行, 纳米通道事件沿微管发生;而进一步筛选发现,线粒体外膜蛋白Miro2同时定位于线粒体间纳米通道与微管伴行部位。调控Miro2蛋白表达显著影响线粒体纳米通道事件发生频率、线粒体间通讯速率、以及线粒体和细胞的呼吸功能。
此外,课题组证实在心肌肥厚时,Miro2蛋白通过Parkin依赖的泛素蛋白酶体途径降解增加,Miro2蛋白水平降低,导致线粒体间通讯事件及线粒体通讯速率降低;而Miro2转基因小鼠则显著增加心肌肥厚时线粒体间的通讯速率、改善线粒体和心脏功能。
该项研究首次阐述了Miro2蛋白在心脏中的保护作用及其作用机制,为心肌肥厚的临床治疗提供了潜在的作用靶点。
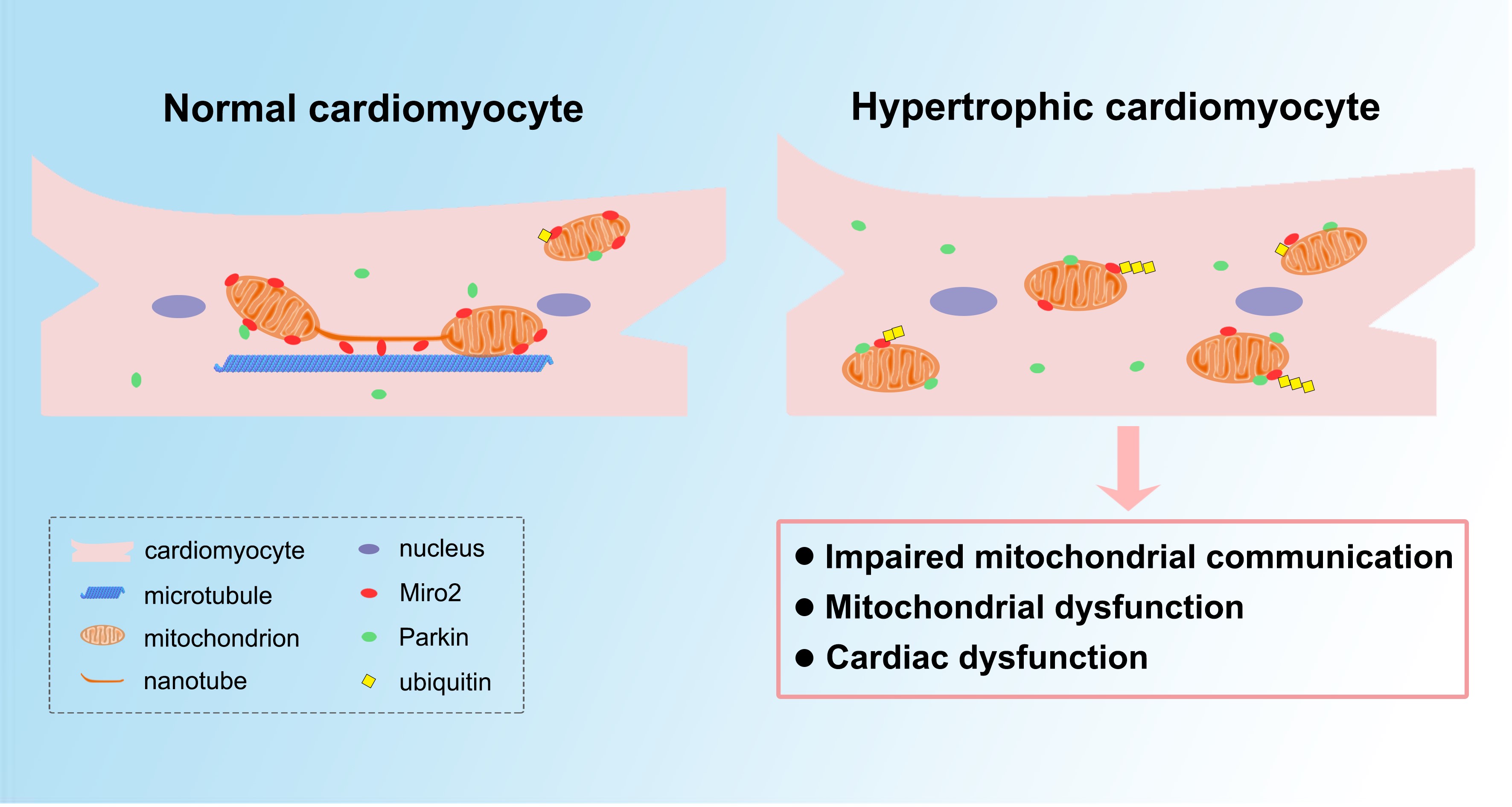
Miro2 mediated inter-mitochondrial communication in cardiomyocytes
郑铭教授为该文通讯作者,基础医学院14级直博生曹阳坡为该文第一作者。本研究得到国家重点基础研究发展规划项目及国家自然科学基金的经费资助。
在线文章链接:https://www.ahajournals.org/doi/abs/10.1161/CIRCRESAHA.119.315432
文章将作为封面文章在9月27日正式发表。

版权与免责声明:本网页的内容由收集互联网上公开发布的信息整理获得。目的在于传递信息及分享,并不意味着赞同其观点或证实其真实性,也不构成其他建议。仅提供交流平台,不为其版权负责。如涉及侵权,请联系我们及时修改或删除。邮箱:sales@allpeptide.com