韩家淮教授课题组发现Rip3的蛋白磷酸酶Ppm1b
3月9日,韩家淮教授课题组在最新一期Nature子刊《Nature Cell Biology》上发表了题为“Ppm1b negatively regulates necroptosis through dephosphorylating Rip3”的研究论文。该研究发现蛋白磷酸酶Ppm1b 通过去磷酸化RIP3负调控程序性细胞坏死(necroptosis),阐明了RIP3磷酸化状态的精确调控对于细胞和机体在生理和病理状态下的存活至关重要。
细胞坏死在发育,宿主抵抗,炎症,肿瘤等多种生理和病理过程中发挥着重要作用。Rip3作为细胞坏死的关键性开关分子,在近几年受到广泛的研究,但是Rip3的磷酸化调控却不为人所知。
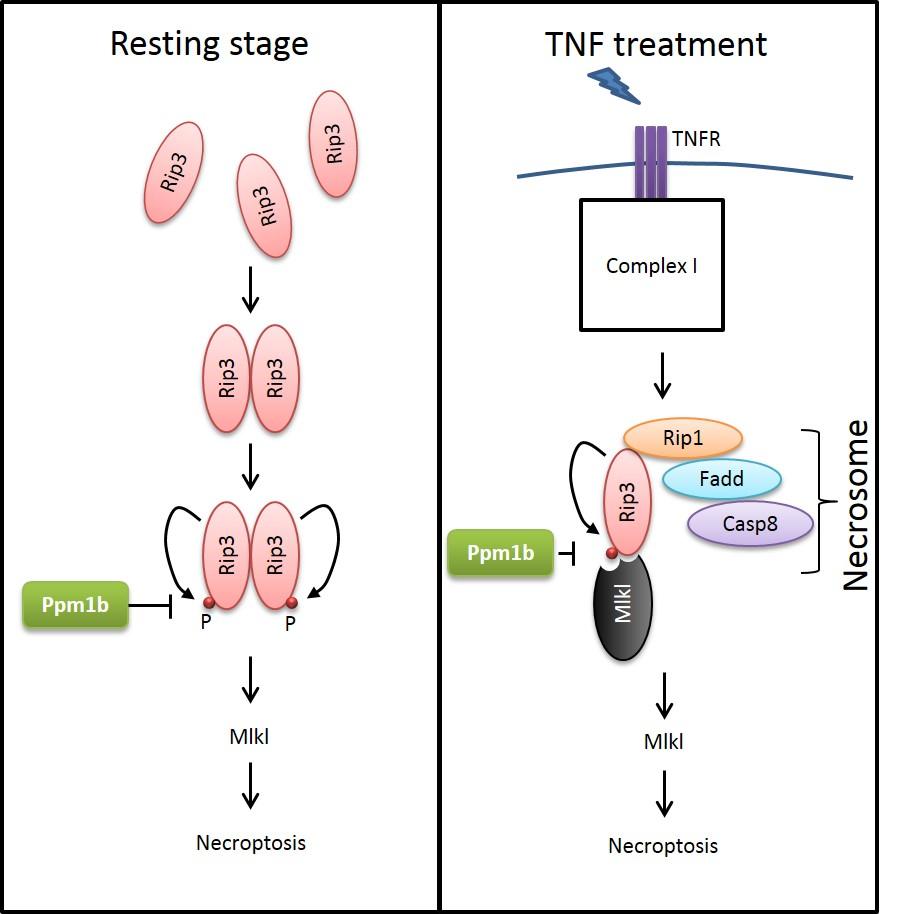
韩家淮教授课题组运用质谱技术分析RIP3免疫共沉淀复合体鉴定出了磷酸酶Ppm1b,第一次证实了RIP3的磷酸化状态是受到细胞精确调控的。该研究发现,在细胞没有受到信号刺激的情况,Ppm1b通过和RIP3的相互作用抑制RIP3的自激活从而促进细胞存活;在受到程序性坏死因子刺激下,Ppm1b通过去磷酸化Rip3从而抑制程序性细胞坏死。进一步研究发现,在肿瘤坏死因子诱导的全身炎症反应综合征的小鼠模型中,Ppm1b能够通过去磷酸化RIP3从而减少小鼠的盲肠损伤并提高小鼠的存活率。由此可见, RIP3磷酸化状态的精确调控对于细胞和机体在生理和病理状态下的存活至关重要。该研究结果为我们治疗由于过量分泌肿瘤坏死因子导致的全身炎症反应综合征提供了一个全新视觉,对于治疗该疾病有这重要的意义。
该文章的第一作者为博士生陈万泽,韩家淮为文章的通讯作者。
(生科办)
版权与免责声明:本网页的内容由收集互联网上公开发布的信息整理获得。目的在于传递信息及分享,并不意味着赞同其观点或证实其真实性,也不构成其他建议。仅提供交流平台,不为其版权负责。如涉及侵权,请联系我们及时修改或删除。邮箱:sales@allpeptide.com