| 编号: | 150318 |
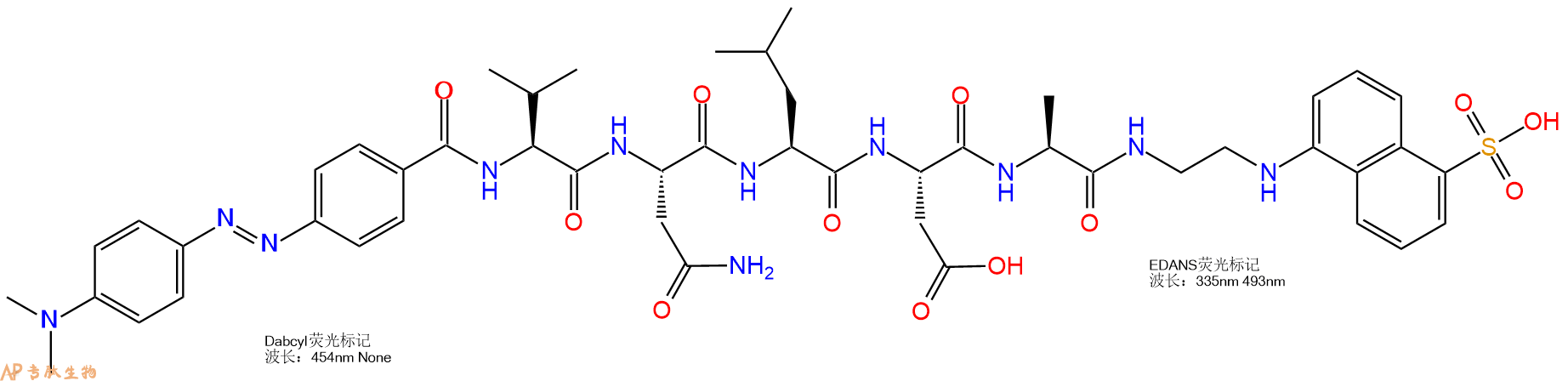
| 中文名称: | 淀粉肽DABCYL-(Asn670, Leu671)-Amyloidbeta/A4 Protein |
| 英文名: | DABCYL-(Asn670, Leu671)-Amyloidbeta/A4 Protein Pre |
| 单字母: | Dabcyl-VNLDA-EDANS |
| 三字母: | DABCYL N端Dabcyl标记 -Val缬氨酸 -Asn天冬酰胺 -Leu亮氨酸 -Asp天冬氨酸 -Ala丙氨酸 -EDANSEDANS |
| 氨基酸个数: | 5 |
| 分子式: | C49H63N11O12S1 |
| 平均分子量: | 1030.16 |
| 精确分子量: | 1029.44 |
| 等电点(PI): | - |
| pH=7.0时的净电荷数: | -1 |
| 平均亲水性: | -0.12 |
| 疏水性值: | 0.56 |
| 外观与性状: | 白色粉末状固体 |
| 消光系数: | - |
| 来源: | 人工化学合成,仅限科学研究使用,不得用于人体。 |
| 纯度: | 95%、98% |
| 盐体系: | 可选TFA、HAc、HCl或其它 |
| 储存条件: | 负80℃至负20℃ |
| 标签: | 荧光共振能量转移肽(FRET) DABCYL标记肽 淀粉样肽(Amyloid Peptides) |
荧光标记所依赖的化合物称为荧光物质。荧光物质是指具有共轭双键体系化学结构的化合物,受到紫外光或蓝紫光照射时,可激发成为激发态,当从激发态恢复基态时,发出荧光。荧光标记技术指利用荧光物质共价结合或物理吸附在所要研究分子的某个基团上,利用它的荧光特性来提供被研究对象的信息。荧光标记的无放射物污染,操作简便等优点,使得荧光标记物在许多研究领域的应用日趋广泛。人们利用利用荧光标记的多肽来检测目标蛋白的活性,并将其发展的高通量活性筛选方法应用于疾病治疗靶点蛋白的药物筛选和药物开发(例如,各种激酶、磷酸酶、肽酶等)。专肽生物经过长期开发,能够提供技术成熟的各种荧光标记多肽。
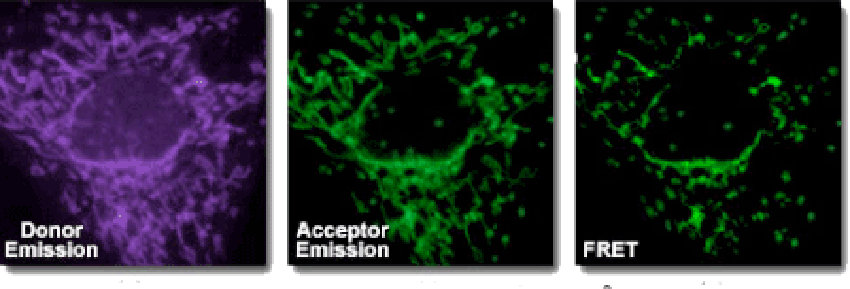
荧光共振能量转移(FRET)是一种非辐射能量跃迁,通过分子间的电偶极相互作用,将供体激发态能量转移到受体激发态的过程。此过程没有光子的参与,所以是非辐射的。该分析方法具有快速、敏感和简单等优点。
用于FRET试验的染料是可以相同的。但在大多数应用中其实是使用不同的染料。例如,一个供体基团(EDANS)和接受基因(DABCYL)匀被连接到一HIV蛋白酶的天然底物上,当该底物未被切断时,DABCYL可淬灭EDANS,从而检测不到荧光。当该底物被HIV-1蛋白酶切断后,EDANS不再被DABCYL淬灭,随即可检测到EDANS荧光。蛋白酶抑制剂的有效性可凭借EDANS荧光强度的变化进行监测。
FRET肽是研究肽酶特异性的便利工具,由于其反应过程可被连续监测,为酶活性的检测提供了一个便捷的方法。供体/受体对的肽键水解后产生的荧光可衡量纳摩尔级浓度的酶活性。当FRET肽是完整的,表现出的是内部的荧光猝灭,但当供体/受体对的任何肽键断裂就会释放出荧光,此荧光可被连续检测,从而可对酶的活性进行定量分析。FRET 肽可作为各类酶研究的合适底物,比如:肽酶、蛋白酶、激酶、磷酸酶的动力特征和功能特征;对新的蛋白水解酶的筛选和检测;对多肽折叠的构象研究等。
1、常用FRET的标准染料组合。
| 常用FRET的标准染料组合 |
| FAM/Lys(Dabcyl) |
| FAM/TAMRA |
| MCA/Lys(Dnp) |
| Abz/Tyr (NO2) |
| Abz/Dnp |
| Abz/EDDnp |
| Dabcyl/Glu(EDANS) |
| Dansyl//Glu(EDANS) |
2、FRET共振能量转移引发荧光猝灭的激发与发射波
| 猝灭剂 | 荧光团 | 激发波(nm) | 发射波(nm) |
| Dabcyl | Edans | 336 | 490 |
| Dansyl | Trp | 336 | 350 |
| DNP | Trp | 328 | 350 |
| DNP | MCA | 328 | 393 |
| DNP | Abz | 328 | 420 |
| Tyr (NO2) | Abz | 320 | 420 |
3、常规RET供体(Donor)-接受(Aceptor)对的福斯特临界距离(Forster Critical Distance)
| 供体 | 受体 | 福斯特临界距离(nm) |
| Cy5 | Cy5.5 | >8.0 |
| B-Phycoerythrin | Cy5.5 | 7.2 |
| FITC | Eosin Thiosemicarbazide | 6.1-6.4 |
| Rhodamine 6G | Malachite Green | 6.1-6.4 |
| BODIPY FL (1) | BODIPY FL (1) | 5.7 |
| GFP | YFP | 5.5-5.7 |
| Cy3 | Cy5.5 | 5 |
| Fluorescein | Tetramethylrhodamine | 4.9-5.5 |
| CF (2) | Texas Red | 5.1 |
| CFP | GFP | 4.7-4.9 |
| Dansyl | Octadecylrhodamine | 4.3 |
| Dansyl | FITC | 3.3-4.1 |
| BFP | DsRFP | 3.1-3.3 |
| IAEDANS (4) | DDPM (3) | 2.5-2.9 |
| Tryptophan | Dansyl | 2.1 |
| (1): 4,4-difluoro-4-bora-3a, 4a-diaza-s-indacene | ||
| (2): carboxyfluorescein succinimidyl ester | ||
| (3): N-(4-dimethylamino-3,5-dinitrophenyl) maleimide | ||
| (4): 5-(2-iodoacetylaminoethyl)aminonaphthalene-1-sulfonic acid | ||
对于分子生物学来讲,生物分析手段的发展,是阐明机理的必要条件。在研究分子间相互作用的道路上,人们不断探索,总结出很多方法,免疫技术,晶体衍射,核磁共振等。1948年,荧光共振能量转移(Fluorescence resonance energy transfer,FRET)理论被首次提出,它可以测定1.0-6.0nm距离内分子间的相互作用。1967年,这一理论得到了实验验证,将1.0-6.0nm的距离称为光学尺。二十世纪八十年代出,通过科学家的不断探索,Fret技术成功运用到蛋白质结构的研究中。自Fret荧光共振能量技术诞生以来,已结合多种先进的技术和方法,如电子显微镜,X射线衍射等,推动了分子生物学检测手段的发展。
荧光共振能量转移技术,是采用物理方法去检测分子间的相互作用的方法。他适用于在细胞正常的生理条件下,验证已知分子间是否存在相互作用。此方法的检测原理如下;
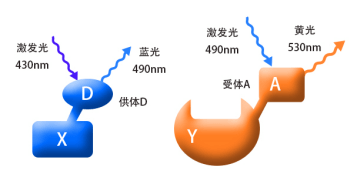
将我们要检测的蛋白(如图X和Y),分别偶联上D和A荧光蛋白,D和A是一对荧光物质,我们称之为供体(donor)和受体(acceptor)。当用430nm的紫光去激发X融合蛋白时,它能够产生490nm的蓝色荧光;同样,当我们用490nm的蓝光去激发Y融合蛋白时,它能够产生530nm的黄色荧光。(结合图1) 。
当蛋白X和Y间没有相互作用时(两者的空间距离>10nm),融合蛋白X和Y分别产生相应的荧光而被检测到,
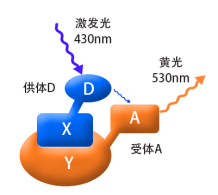
如果蛋白X和Y间存在相互作用(两者的空间距离需<10nm,结合图2),用紫光激发融合蛋白X其产生的蓝光会被融合蛋白Y吸收,从而产生黄色荧光,这时,在细胞内将检测不到蓝色荧光的存在。这时因为能量从X融合蛋白转移到了Y融合蛋白,这就是荧光共振能量转移技术。
一个理想的Fret相互作用体系,要求要有一对合适的荧光物质, 即供体的发射光谱与受体的吸收光谱有明显的重叠。且当供体的激发波长时对受体无影响,供体和受体的发射光谱要完全分开,否则容易造成光谱干涉,而使反应体系不稳定。目前,较为常用的供体-受体分子对,主要有绿色荧光蛋白类(GFPs)和染料类。绿色荧光蛋白类有CFP-YFP,BFP-GFP,BFP-YFP等,染料类的有Cy3-Cy5,FITC-Rhodamine等。且这些荧光物质要能够标记在研究对象上。
| 优点 | 缺点 |
| 在活细胞的正常生理条件下进行检测,观察大分子在细胞内的构象变化与相互作用,并弥补了需破碎细胞检测相互作用的缺点 | 应用比较局限,一般需要在待检测分子上偶联荧光物质(加上标记) |
| 灵敏度高,可实现对单细胞水平的研究,研究单个受体分子 | 对实验要求较高,如供受体的光谱重叠不好,会导致荧光干扰,对供受体的抗干扰能力,水溶性等要求高 |
| 可与多种仪器和技术结合使用,如显微镜,色谱技术,电泳,流失细胞技术等 | 需要不断探索合适的供体和受体,且能够标记分子 难以观察瞬时的分子间作用,检测要求大量的样品 |
以荧光物质CFP(供体)-YFP(受体)为例,检测AB蛋白在细胞内的相互作用。
最常见的一对标记组合是 Dancyl和Edans,
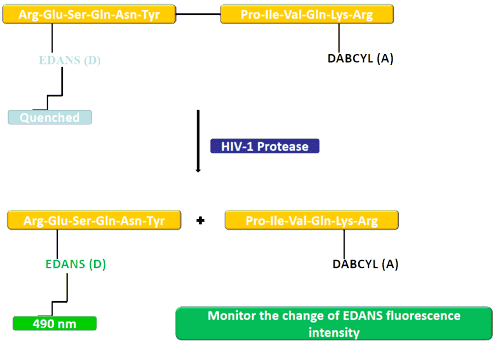
在本例中,荧光团 (EDANS) 和猝灭剂 (DABCYL) 与 HIV 蛋白酶的天然底物相连。在未裂解的底物中,DABCYL 淬灭 EDANS,因此没有可检测到的荧光。底物被 HIV-1 蛋白酶切割后,DABCYL 不再淬灭 EDANS,从而检测到 EDANS 荧光。然后可以监测 EDANS 荧光强度的变化以评估蛋白酶抑制剂的效率。
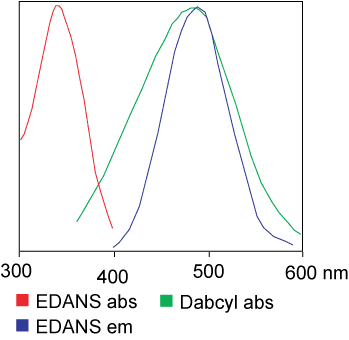
FRET 肽可用于研究肽酶特异性,因为它们可以连续监测反应,从而快速确定酶活性。供体/受体对之间的肽键可以被切割,从而产生荧光信号以测量纳摩尔浓度的酶活性。当未被切割时,FRET 肽会淬灭内部荧光;然而,供体/受体对之间肽键的断裂会释放出可以连续检测到的荧光信号,从而可以量化酶的活性。
FRET 肽在许多不同的酶研究中用作合适的底物:
肽酶、蛋白酶、激酶和磷酸酶的动力学和功能表征。
筛选和检测新型蛋白水解酶。
肽折叠的构象研究。
多肽荧光标记由于没有放射性,实验操作简单。因此,目前在生物学研究中多肽荧光标记应用非常广泛,多肽荧光标记方法与荧光试剂的结构有关系,对于有游离羧基的采用的方法与接多肽反应相同,也采用HBTU/HOBt/DIEA方法连接。 在N端标记FITC的多肽需经历环化作用来形成荧光素,通常会伴有最后一个氨基酸的去除,但当有一个间隔器如氨基己酸,或者是通过非酸性环境将目的多肽从树脂上切下来时,这种情况可避免在切割的过程中被TFA切割掉。
人们利用利用荧光标记的多肽来检测目标蛋白的活性,并将 其发展的高通量活性筛选方法应用于疾病治疗靶点蛋白的药物筛选和药物开发(例如,各种激 酶、磷酸酶、肽酶等)。
专肽生物能够提供技术成熟的各种荧光标记多肽。
下面是一些常见的多肽修饰荧光物质结构:
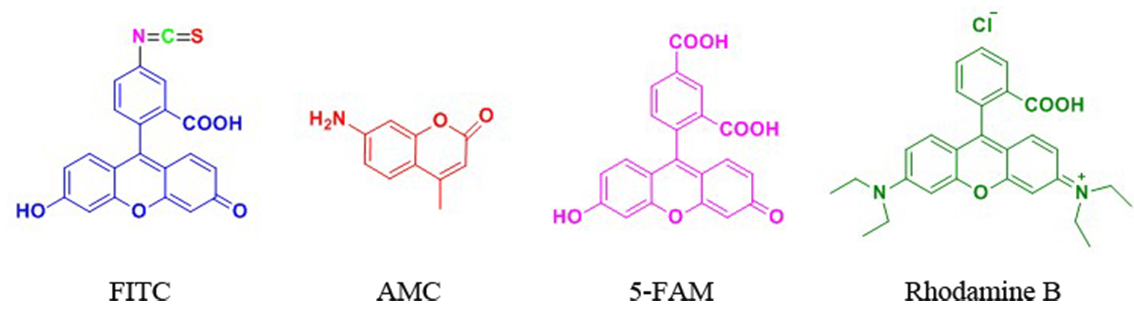
FITC标记
FITC(异硫氰酸荧光素)具有比较高的活性,我们公司可以通过两种方式将FITC标记于多肽 上:(1) 将FITC标记于赖氨酸(Lys)或被选择性地脱保护的鸟氨酸(ornithine)侧链氨基 上;(2) 将FITC标记于多肽N端氨基。
当在N端标记时,建议在最后一个氨基和由异硫氰酸酯与氨基反应产生的硫脲键之间引入 烷基间隔器(alkyl spacer),如氨基己酸(Ahx)。链接切割需要酸性环境,在N端标记FITC 的多肽需经历环化作用来形成荧光素,通常会伴有最后一个氨基酸的去除,但当有一个间隔器 如氨基己酸,或者是通过非酸性环境将目的肽从树脂上切下来时,这种情况可避免。空间位阻 被认为是在荧光染料前使用Ahx的主要原因,而不是为什么FITC不能直接偶联在多肽上的原因。
Ahx或b-Ala均可作为间隔器用于FITC标记的多肽上。

| 荧光修饰中文名称 | N端 | N端带有linker |
| 生物素标记多肽 | Biotin- | Biotin-Ahx- |
| 异硫氰酸荧光素 | FITC- | FITC-Ahx- |
| 5-羧基荧光素 | 5-FAM- | 5-FAM-Ahx- |
| 丹磺酰荧光素 | Dansyl- | Dansyl-Ahx- |
| 5-羧基四甲基罗丹明 | TMR- (TAMRA-) | TMR-Ahx- (TAMRA-Ahx-) |
| 多肽N端 | 多肽序列中间 | N端带有linker |
| 生物素标记多肽 | Biotin- | 多肽C端 |
| Lys(Biotin)- | -Lys(Biotin)-- | -Lys(Biotin) |
| Lys(FITC)- | -Lys(FITC)- | -Lys(FITC) |
| Lys(5-FAM)- | -Lys(5-FAM)- | -Lys(5-FAM) |
| Lys(Dansyl)- | -Lys(Dansyl)- | -Lys(Dansyl) |
| Lys(TMR)- | -Lys(TMR)- | -Lys(TMR) |
| Lys(Dnp)- | -Lys(Dnp)- | -Lys(Dnp) |
专肽常做的荧光物质的激发光波长和发射光波长。可供参考选择:
| 荧光基团 | Ex(nm) | Em(nm) | 荧光基团 | Ex(nm) | Em(nm) |
| 羟基香豆素 | 325 | 386 | R-phycoerythrin (PE) (489) | 565 | 578 |
| 丹磺酰氯 | 340 | 578 | Rhodamine Red-X | 560 | 580 |
| AMC | 345 | 445 | Tamara | 565 | 580 |
| 甲氧基香豆素 | 360 | 410 | Alexa fluor 555 | 556 | 573 |
| Alexa fluor 系列 | 345 | 442 | Alexa fluor 546 | 556 | 573 |
| 氨基香豆素 | 350 | 445 | Rox | 575 | 602 |
| Dabcyl | 453 | - | Alexa fluor 568 | 578 | 603 |
| Cy2 | 490 | 510 | Texas Red | 589 | 615 |
| FAM | 495 | 517 | Alexa fluor 594 | 590 | 617 |
| Alexa fluor 488 | 494 | 517 | Alexa fluor | 621 | 639 |
| FITC | 495 | 519 | Alexa fluor 633 | 650 | 668 |
| Alexa fluor 430 | 430 | 545 | Cy5 (625) | 650 | 670 |
| 5-FAM | 492 | 518 | Alexa fluor 660 | 663 | 690 |
| Alexa fluor 532 | 530 | 530 | Cy5.5 | 675 | 694 |
| HEX | 535 | 556 | TruRed | 490; 675 | 695 |
| 5-TAMRA | 542 | 568 | Alexa fluor 680 | 679 | 702 |
| Cy3 | 550 | 570 | Cy7 | 743 | 767 |
| TRITC | 547 | 572 | Cy3.5 | 581 | 596 |
淀粉肽背景:β淀粉样蛋白(Aβ或Abeta)是从淀粉样前体蛋白加工而成的含有36–43个氨基酸的多肽。Aβ是与阿尔兹海默病相关的淀粉样蛋白斑的成分。已有证据表明,Aβ是一个多功能肽,具有显著的非病理性活性。Aβ是阿尔兹海默病患者脑中发现的沉积物的主要成分。在散发性阿尔兹海默病患者的脑中,Aβ的水平升高,造成脑血管病变和神经毒性。Aβ蛋白是由β和γ分泌酶的连续作用而产生的。γ分泌酶产生Aβ肽的C末端,在APP的转膜结构域切割,可以产生许多36-43个氨基酸残基长度的异构体,最常见的异构体是Aβ40和Aβ42。更长形式的Aβ在内质网中切割产生,而更短形式的Aβ在反面高尔基网中产生。
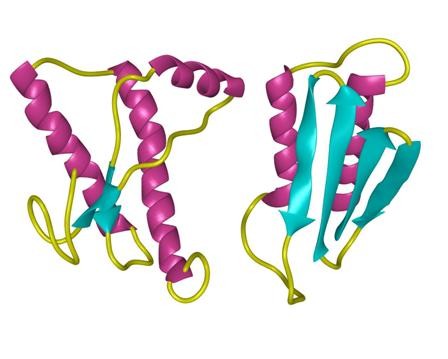
structure of Amyloid β-Peptide (1-40) (human)
淀粉样蛋白肽的 定义淀粉样蛋白 是丝状蛋白质沉积物,大小从纳米到微米不等,并且由肽β链的平行或反平行排列形成的聚集的肽β折叠构成。
结构特征:使用固态NMR(SSNMR),与计算能量最小化过程结合,Tycko和合作者已经提出从淀粉状蛋白肽SS(Aß1-40)的40个残基的形式形成的淀粉样蛋白原纤维的结构在pH 7.4和24 o C在静止条件下。在这种结构中,每个Aß1-40分子在原纤维的核心区域贡献一对ß链,大约跨越残基12-24和30-40。这些由回路25-29连接的链不是同一张ß-sheet的一部分,但参与同一原丝内两个不同的ß-sheets的形成。不同的Aß分子2、3至少从第9到39位残基以平行排列和对齐的方式相互堆叠。通过调用其他实验约束,例如使用透射电子显微镜(TEM)观察到的原丝直径和单位质量通过扫描透射电子显微镜(STEM)1、2测得的长度表明,单个原丝是由四个ß片组成的,它们之间的距离约为10Å。
作用模式:阿尔茨海默氏病(AD)是淀粉样蛋白丝状沉积物的结果,淀粉状蛋白沉积物在分子水平上定义该疾病,发生在神经周膜,轴突,树突和神经元末端,如神经原纤维缠结(NFT),在细胞外神经纤维中淀粉样斑块(APC),以及周围的血管称为淀粉样嗜血性血管病(ACA)。淀粉样蛋白沉积物显然发生在发展NFT的神经元末端区域。已经表明,APC和ACA的主要成分已被证明是4.5kDa的淀粉样蛋白,最初被称为“β-蛋白”或“淀粉样蛋白A4”,我们现在将其称为“βA4”。
功能:钙失调和膜破坏是可溶性淀粉样蛋白低聚物普遍存在的神经毒性机制:进行了一项研究,以研究Ca 2+信号转导可能参与淀粉样蛋白诱导的细胞毒性,疾病相关淀粉样蛋白(β,病毒,胰岛淀粉样蛋白)的均质制剂制备了处于各种聚集状态的多肽,聚谷氨酰胺和溶菌酶),并测试了它们对加载fluo-3的SH-SY5Y细胞的作用。寡聚形式的所有淀粉样蛋白的应用(0.6-6 µg / ml)迅速(约5 s)使细胞内Ca 2+升高,而等量的单体和原纤维则没有。细胞内Ca 2+耗尽后,Abeta42低聚物引起的Ca 2+信号持续存在店,和小信号仍留在钙2 + -游离介质,指示从细胞外和细胞内Ca贡献2+源。膜对Ca 2+的渗透性增加不能归因于内源性Ca 2+通道的活化,因为反应不受强力的Ca 2 +-通道阻滞剂钴的影响。取而代之的是,观察到Abeta42和其他低聚物引起阴离子荧光染料的快速细胞泄漏,这表明膜通透性普遍提高。导致的离子和分子通量失调可能为许多淀粉样变性疾病中Ca 2+失调提供了由低聚物介导的毒性的常见机制。离子起着至关重要的作用,因为它们的跨膜浓度梯度很强,并且参与了细胞功能障碍和死亡。
2型糖尿病中的胰岛淀粉样蛋白和毒性低聚物假说: 2型糖尿病(T2DM)的特征是胰岛素抵抗,胰岛素分泌缺陷,β细胞量减少,β细胞凋亡增加和胰岛淀粉样蛋白。胰岛淀粉样蛋白源自胰岛淀粉样蛋白多肽(IAPP,胰岛淀粉样多肽),该蛋白是通过胰β细胞与胰岛素共表达和共分泌的蛋白。与其他淀粉样蛋白一样,IAPP具有形成膜渗透性毒性低聚物的倾向。越来越多的证据表明,这些有毒的寡聚体而不是这些蛋白质的细胞外淀粉样蛋白形式,是导致神经退行性疾病中神经元丢失的原因。有人提出,胞内IAPP寡聚物的形成可能会导致T2DM 6中的β细胞丢失。
多肽DABCYL-Val-Asn-Leu-Asp-Ala-EDANS的合成步骤:
1、合成CTC树脂:称取0.91g CTC Resin(如初始取代度约为0.74mmol/g)和0.81mmol Fmoc-Ala-OH于反应器中,加入适量DCM溶解氨基酸(需要注意,此时CTC树脂体积会增大好几倍,避免DCM溶液过少),再加入2.02mmol DIPEA(Mw:129.1,d:0.740g/ml),反应2-3小时后,可不抽滤溶液,直接加入1ml的HPLC级甲醇,封端半小时。依次用DMF洗涤2次,甲醇洗涤1次,DCM洗涤一次,甲醇洗涤一次,DCM洗涤一次,DMF洗涤2次(这里使用甲醇和DCM交替洗涤,是为了更好地去除其他溶质,有利于后续反应)。得到 Fmoc-Ala-CTC Resin。结构图如下:
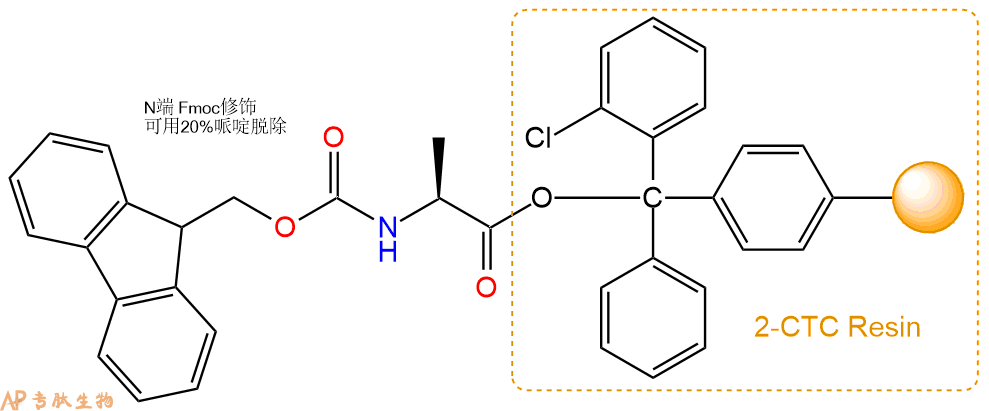
2、脱Fmoc:加3倍树脂体积的20%Pip/DMF溶液,鼓氮气30分钟,然后2倍树脂体积的DMF 洗涤5次。得到 H2N-Ala-CTC Resin 。(此步骤脱除Fmoc基团,茚三酮检测为蓝色,Pip为哌啶)。结构图如下:
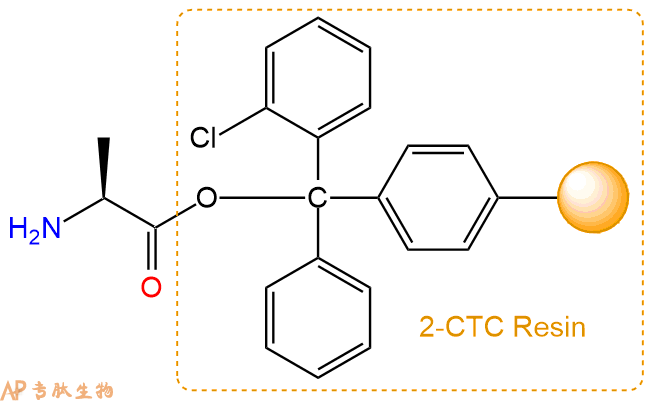
3、缩合:取2.02mmol Fmoc-Asp(OtBu)-OH 氨基酸,加入到上述树脂里,加适当DMF溶解氨基酸,再依次加入4.04mmol DIPEA,1.92mmol HBTU。反应30分钟后,取小样洗涤,茚三酮检测为无色。用2倍树脂体积的DMF 洗涤3次树脂。(洗涤树脂,去掉残留溶剂,为下一步反应做准备)。得到Fmoc-Asp(OtBu)-Ala-CTC Resin。氨基酸:DIPEA:HBTU:树脂=3:6:2.85:1(摩尔比)。结构图如下:
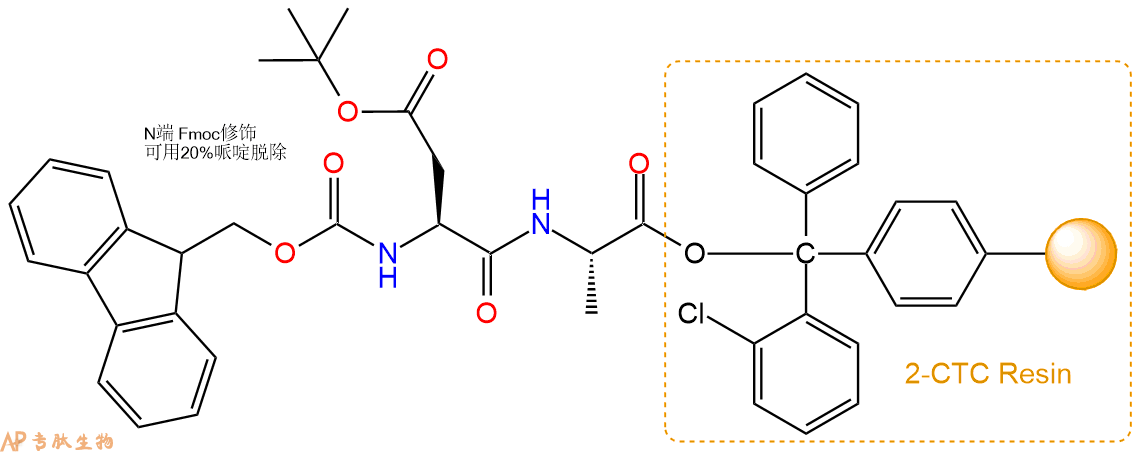
4、依次循环步骤二、步骤三,依次得到
H2N-Asp(OtBu)-Ala-CTC Resin
Fmoc-Leu-Asp(OtBu)-Ala-CTC Resin
H2N-Leu-Asp(OtBu)-Ala-CTC Resin
Fmoc-Asn(Trt)-Leu-Asp(OtBu)-Ala-CTC Resin
H2N-Asn(Trt)-Leu-Asp(OtBu)-Ala-CTC Resin
Fmoc-Val-Asn(Trt)-Leu-Asp(OtBu)-Ala-CTC Resin
以上中间结构,均可在专肽生物多肽计算器-多肽结构计算器中,一键画出。
最后再经过步骤二得到 H2N-Val-Asn(Trt)-Leu-Asp(OtBu)-Ala-CTC Resin,结构如下:
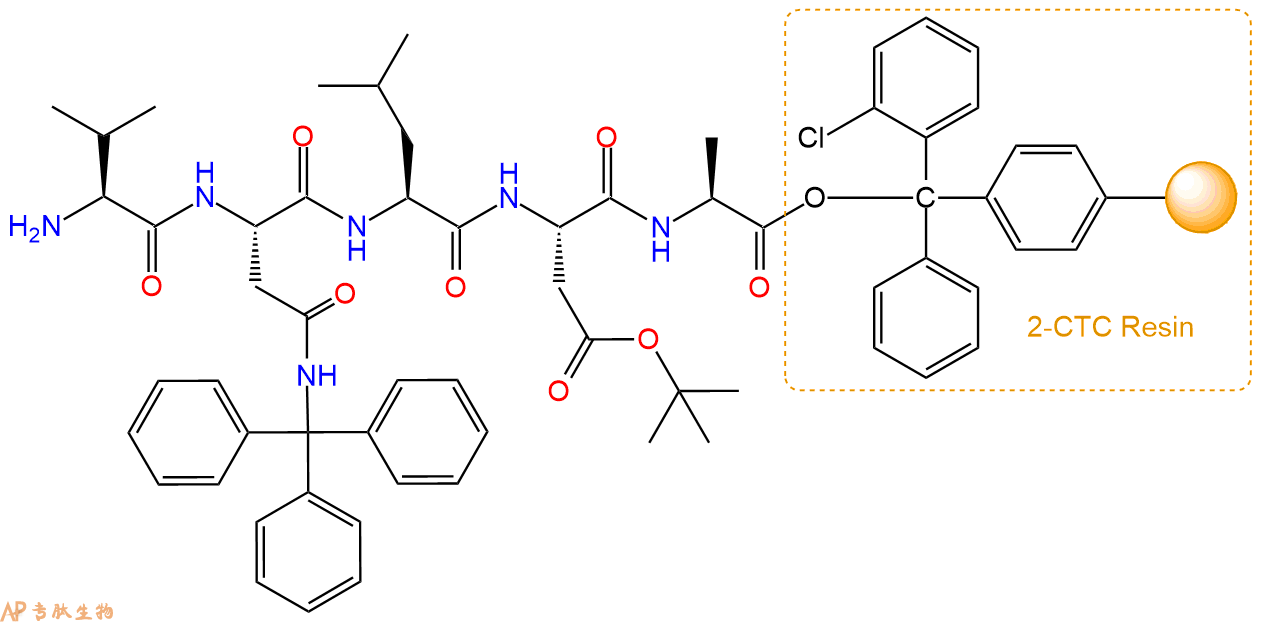
5、4-二甲胺偶氮苯-4’-羧酸(DABCYL)反应连接:在上述树脂中,加入适当DMF后,再加入2.02mmol4-二甲胺偶氮苯-4’-羧酸(DABCYL)到树脂中,再加入4.04mmol DIPEA,鼓氮气反应30分钟。用2倍树脂体积的DMF 洗涤3次树脂(洗涤树脂,去掉残留溶剂,为下一步反应做准备)。 得到DABCYL-Val-Asn(Trt)-Leu-Asp(OtBu)-Ala-CTC Resin。 结构如下:
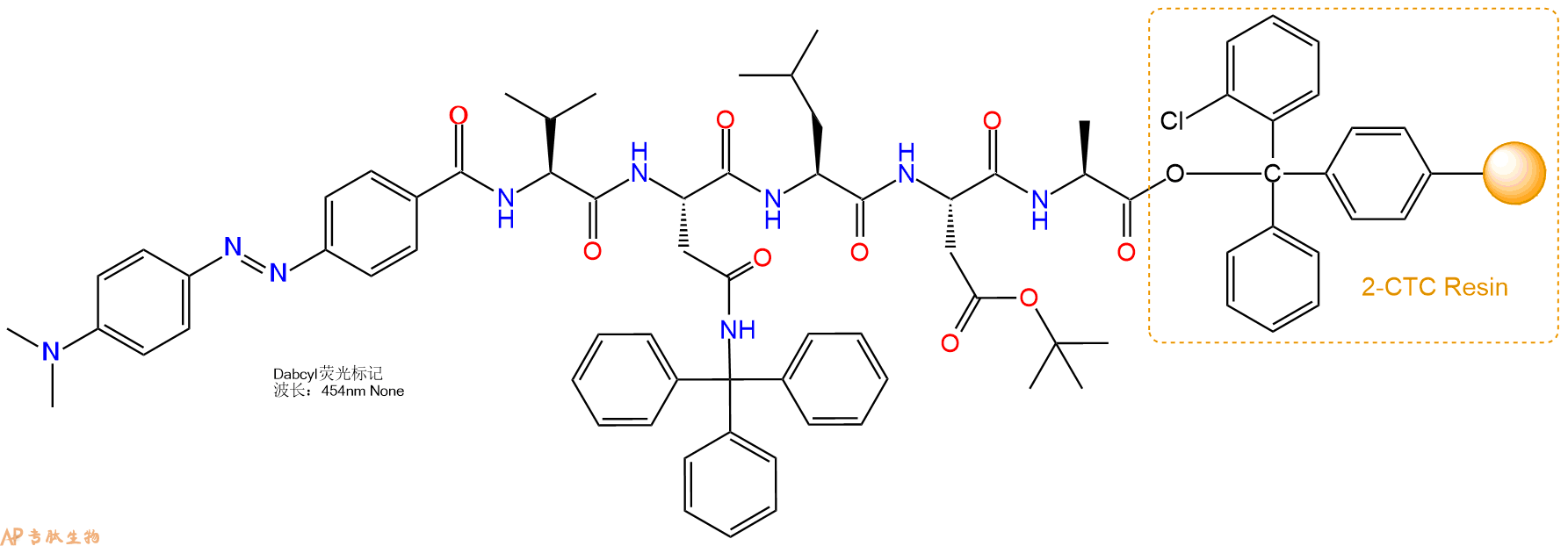
6、全保护切割:配置0.5%TFA/DCM溶液,溶液体积约为树脂体积的3倍。再次用DCM洗涤树脂2遍(去除残留DMF),后将配置好的溶液倒入到反应器中,反应30分钟。抽滤树脂,收集滤液(此时多肽已经从树脂上分离,存在于滤液中)。多肽序列为 DABCYL-Val-Asn(Trt)-Leu-Asp(OtBu)-Ala-CTC Resin。 在滤液中添加DIEPA,调PH至7-8。用饱和NaHCO3洗涤滤液,分离出DCM层溶液。可适当旋蒸DCM层溶液,减少有机溶剂。再次加入1或2倍体积的乙酸乙酯,用稀HCl溶液调PH至微酸性,将多肽从DCM层萃取到乙酸乙酯层。用饱和NaCl洗涤2次乙酸乙酯层。用无水硫酸镁吸收乙酸乙酯层的水分。通过减压旋蒸,直接将乙酸乙酯完全旋蒸掉,得到晶体状固体多肽,用于下一步C端反应。或通过减压旋蒸保留适量乙酸乙酯的溶液体积,加入冰乙醚析出 多肽,然后对多肽进行烘干操作即可用于下一步C端反应。DABCYL-Val-Asn(Trt)-Leu-Asp(OtBu)-Ala-COOH的结构图如下。
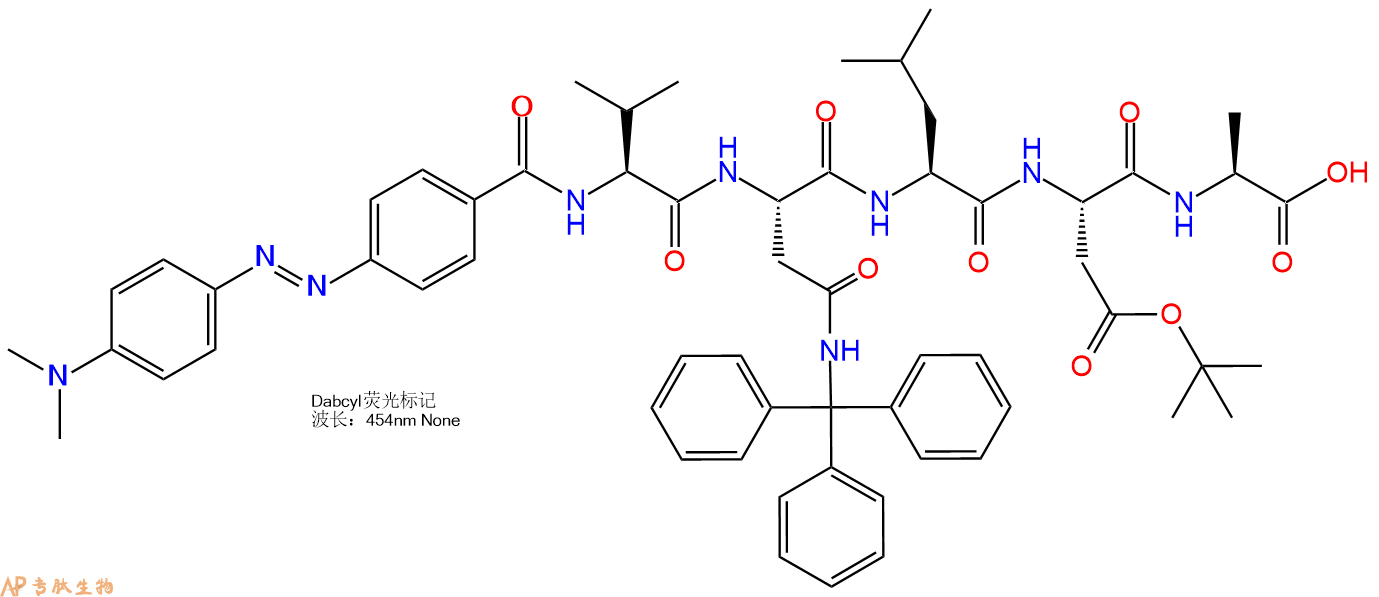
7、5-(2-氨基乙氨基)-1-萘磺酸反应连接:在上述树脂中,加入适当DMF后,再加入2.02mmol 5-(2-氨基乙氨基)-1-萘磺酸到树脂中,再加入4.04mmol DIPEA、1.92mmol HBTU,鼓氮气反应30分钟。用2倍树脂体积的DMF 洗涤3次树脂(洗涤树脂,去掉残留溶剂,为下一步反应做准备)。 得到 DABCYL-Val-Asn(Trt)-Leu-Asp(OtBu)-Ala-EDANS。 结构如下:
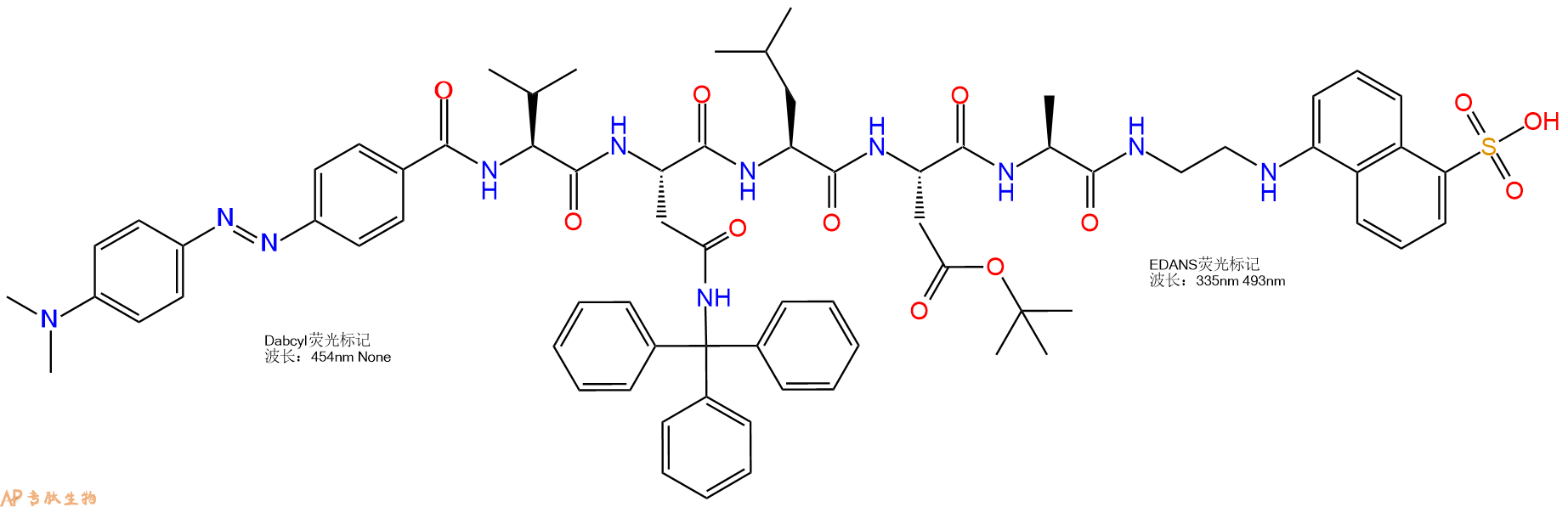
8、切割:6倍树脂体积的切割液(或每1g树脂加8ml左右的切割液),摇床摇晃 2小时,过滤掉树脂,用冰无水乙醚沉淀滤液,并用冰无水乙醚洗涤沉淀物3次,最后将沉淀物放真空干燥釜中,常温干燥24小试,得到粗品DABCYL-Val-Asn-Leu-Asp-Ala-EDANS。结构图见产品结构图。
切割液选择:1)TFA:H2O=95%:5%
2)TFA:H2O:TIS=95%:2.5%:2.5%
3)三氟乙酸:茴香硫醚:1,2-乙二硫醇:苯酚:水=87.5%:5%:2.5%:2.5%:2.5%
(前两种适合没有容易氧化的氨基酸,例如Trp、Cys、Met。第三种适合几乎所有的序列。)
9、纯化冻干:使用液相色谱纯化,收集目标峰液体,进行冻干,获得蓬松的粉末状固体多肽。不过这时要取小样复测下纯度 是否目标纯度。
10、最后总结:
杭州专肽生物技术有限公司(ALLPEPTIDE https://www.allpeptide.com)主营定制多肽合成业务,提供各类长肽,短肽,环肽,提供各类修饰肽,如:荧光标记修饰(CY3、CY5、CY5.5、CY7、FAM、FITC、Rhodamine B、TAMRA等),功能基团修饰肽(叠氮、炔基、DBCO、DOTA、NOTA等),同位素标记肽(N15、C13),订书肽(Stapled Peptide),脂肪酸修饰肽(Pal、Myr、Ste),磷酸化修饰肽(P-Ser、P-Thr、P-Tyr),环肽(酰胺键环肽、一对或者多对二硫键环),生物素标记肽,PEG修饰肽,甲基化修饰肽
以上所有内容,为专肽生物原创内容,请勿发布到其他网站上。





