编号:119754
CAS号:
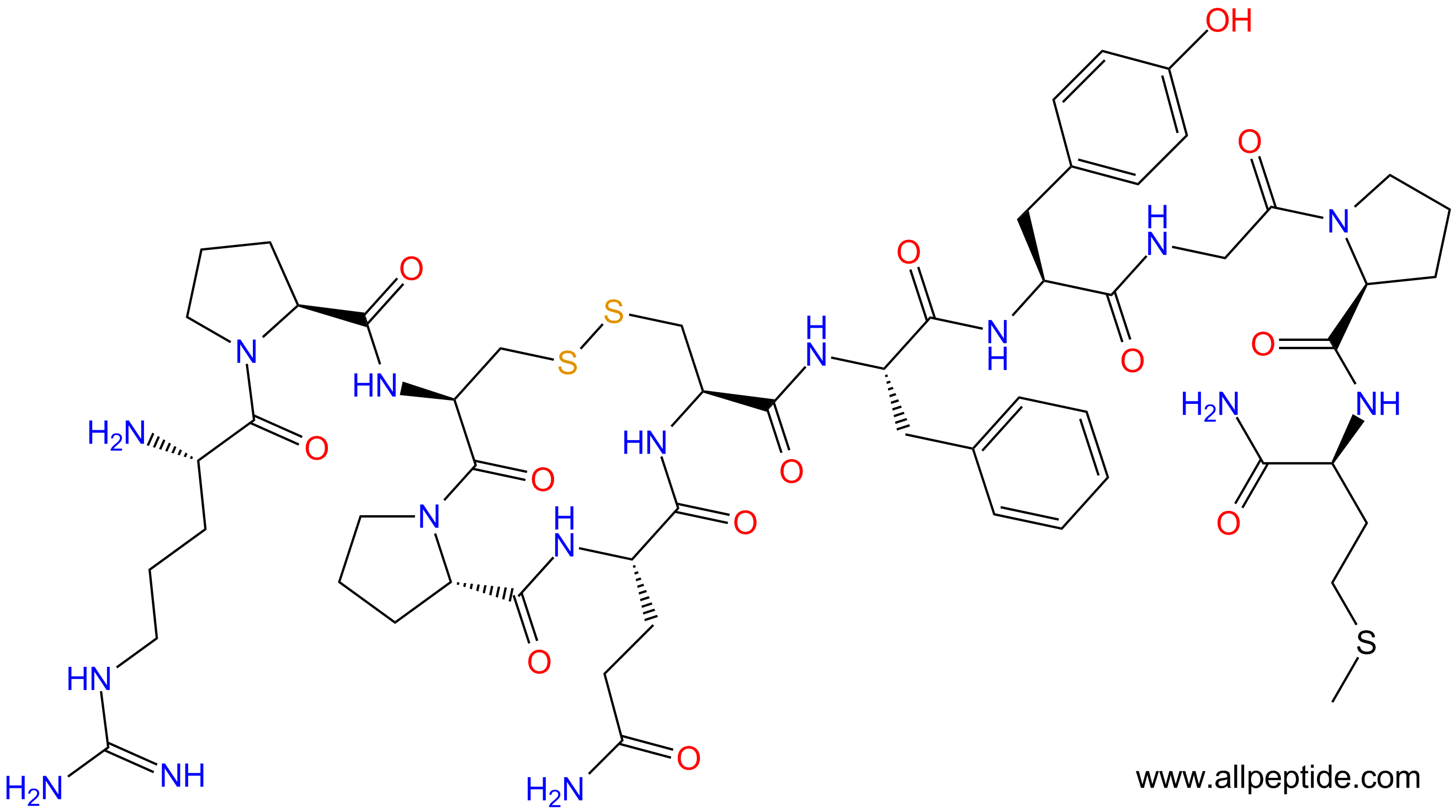
单字母:H2N-RPCPQCFYGPM-NH2(Disulfide Bridge:C3-C6)
| 编号: | 119754 |
| 中文名称: | P物质肽[Cys3, 6, Tyr8, Pro10]- Substance P |
| 英文名: | [Cys3, 6, Tyr8, Pro10]- Substance P |
| 单字母: | H2N-RPCPQCFYGPM-NH2(Disulfide Bridge:C3-C6) |
| 三字母: | H2N-Arg-Pro-Cys-Pro-Gln-Cys-Phe-Tyr-Gly-Pro-Met-NH2(Disulfide Bridge:Cys3-Cys6) |
| 氨基酸个数: | 11 |
| 分子式: | C57H82N16O13S3 |
| 平均分子量: | 1295.56 |
| 精确分子量: | 1294.54 |
| 等电点(PI): | - |
| pH=7.0时的净电荷数: | 4.91 |
| 平均亲水性: | -0.85714285714286 |
| 疏水性值: | -0.4 |
| 外观与性状: | 白色粉末状固体 |
| 消光系数: | 1490 |
| 来源: | 人工化学合成,仅限科学研究使用,不得用于人体。 |
| 纯度: | 95%、98% |
| 盐体系: | 可选TFA、HAc、HCl或其它 |
| 生成周期: | 2-3周 |
| 储存条件: | 负80℃至负20℃ |
| 标签: | 二硫键环肽 P物质及相关肽 |
二硫键广泛存在与蛋白结构中,对稳定蛋白结构具有非常重要的意义,二硫键一般是通过序列中的2个Cys的巯基,经氧化形成。
形成二硫键的方法很多:空气氧化法,DMSO氧化法,过氧化氢氧化法等。
二硫键的合成过程, 可以通过Ellman检测以及HPLC检测方法对其反应进程进行监测。
如果多肽中只含有1对Cys,那二硫键的形成是简单的。多肽经固相或液相合成,然后在pH8-9的溶液中进行氧化。
当需要形成2对或2对以上的二硫键时,合成过程则相对复杂。尽管二硫键的形成通常是在合成方案的最后阶段完成,但有时引入预先形成的二硫化物是有利于连合或延长肽链的。通常采用的巯基保护基有trt, Acm, Mmt, tBu, Bzl, Mob, Tmob等多种基团。我们分别列出两种以2-Cl树脂和Rink树脂为载体合成的多肽上多对二硫键形成路线:
二硫键反应条件选择
二硫键即为蛋白质或多肽分子中两个不同位点Cys的巯基(-SH)被氧化形成的S-S共价键。 一条肽链上不同位置的氨基酸之间形成的二硫键,可以将肽链折叠成特定的空间结构。多肽分 子通常分子量较大,空间结构复杂,结构中形成二硫键时要求两个半胱氨酸在空间距离上接近。 此外,多肽结构中还原态的巯基化学性质活泼,容易发生其他的副反应,而且肽链上其他侧链 也可能会发生一系列修饰,因此,肽链进行修饰所选取的氧化剂和氧化条件是反应的关键因素, 反应机理也比较复杂,既可能是自由基反应,也可能是离子反应。
反应条件有多种选择,比如空气氧化,DMSO氧化等温和的氧化过程,也可以采用H2O2,I2, 汞盐等激烈的反应条件。
空气氧化法: 空气氧化法形成二硫键是多肽合成中最经典的方法,通常是将巯基处于还原态的多肽溶于水中,在近中性或弱碱性条件下(PH值6.5-10),反应24小时以上。为了降低分子之间二硫键形成的可能,该方法通常需要在低浓度条件下进行。
碘氧化法:将多肽溶于25%的甲醇水溶液或30%的醋酸水溶液中,逐滴滴加10-15mol/L的碘进行氧化,反应15-40min。当肽链中含有对碘比较敏感的Tyr、Trp、Met和His的残基时,氧化条件要控制的更精确,氧化完后,立即加入维生素C或硫代硫酸钠除去过量的碘。 当序列中有两对或多对二硫键需要成环时,通常有两种情况:
自然随机成环: 序列中的Cys之间随机成环,与一对二硫键成环条件相似;
定点成环: 定点成环即序列中的Cys按照设计要求形成二硫键,反应过程相对复杂。在 固相合成多肽之前,需要提前设计几对二硫键形成的顺序和方法路线,选择不同的侧链 巯基保护基,利用其性质差异,分步氧化形成两对或多对二硫键。 通常采用的巯基保护 基有trt, Acm, Mmt, tBu, Bzl, Mob, Tmob等多种基团。
定义
物质P(SP)是十一肽,在周围和中枢神经系统中都丰富,通常与一种经典的神经递质之一,最常见的是血清素(5-HT)1共定位。
相关肽
SP属于神经肽家族,称为速激肽,具有共同的C端序列:Phe-X-Gly-Leu-Met-NH 2。三种最常见的速激肽是SP,神经激肽A(NKA)和神经激肽B(NKB)。它们的生物学作用是通过称为NK1,NK2和NK3的特定细胞表面受体介导的,其中SP是NK1受体的首选激动剂,NKA是NK2受体的首选激动剂,NKB是NK3受体的2激动剂。
Discovery
SP最初是由冯·欧拉(von Euler)和加德姆(Gaddum)于1931年发现的,是一种引起体外肠道收缩的组织提取物。在随后的几十年中,它的生物活性和组织分布得到了进一步的研究3。
结构特征
SP是具有11个残基的神经肽,序列为Arg-Pro-Lys-Pro-Gln-Glin-Phe-Gly-Leu-Met-NH 2)4。在一项研究中,将SP的C和N末端片段与母体分子在以下方面的能力进行了比较:(a)收缩分离的豚鼠回肠,(b)在大鼠中诱导唾液分泌,(c)激发单只猫背角神经元,以及(d)通过小鼠颅内注射诱导抓挠。在所有测定系统中,与七肽一样小的C末端片段都是有效的SP激动剂。包含五个或更少氨基酸的C末端片段至多仅具有弱活性。N-末端片段在分离的豚鼠回肠上完全没有活性。然而,在大鼠唾液分泌和中枢神经系统分析中,N末端片段具有弱的SP样活性5。获得的结果表明,尽管SP的羧基末端对于肽支气管活性是必不可少的,但是氨基末端肽的丢失(最多四个残基)实际上增强了对肽的支气管收缩剂反应。这种增强的一部分似乎是由SP和SP5-11的酶促降解差异引起的。数据表明,二肽基氨基肽酶对SP的切割可以增强其生物活性6。SP类似物:Senktide(琥珀酰-[Asp6,Me-Phe8] SP-(6-11))是NK-3(SP-N)受体的选择性类似物,效力比SP高20-100倍,约为1000倍比为NK-1(SP-P)受体选择性类似物,其驻留在肌肉细胞更有效的7。鞘内注射后研究了5种SP类似物对神经激肽(NK)1受体激动剂如SP,藻蛋白和(p-Glu6,Pro9)-SP(6-11)(肽)诱导的舔,咬和scratch痒反应的影响。在小鼠中。肽引起类似SP的行为反应,其效力是D-Pro9类似物D-肽的25倍。(D-Arg1,D-Pro2,4,D-Phe7,D-His9,Leu11)-SP的剂量低于(D-Phe7,D-His9,Leu11)-SP的肽诱导的应答(6 -11)。相反,(D-Arg1,D-Pro2,4,D-Phe7,D-His9)-SP(0.5-1.0 nmol)和(D-Phe7,D-His9)-SP(6-11)(0.5- 2.0 nmol)仅抑制SP诱导的行为反应,而不抑制physalaemin或肽诱导的反应。8。P物质[D-Arg1,D-Phe5,D-Trp7,9,Leu11] SP(SpD)和[Arg6,D-Trp7,9,NmePhe8]类似物P可以抑制神经肽刺激的Ca2 +动员,酪氨酸磷酸化和ERK激活。至关重要的是,SpD和[Arg6,D-Trp7,9,NmePhe8] SP在体内和体外均抑制SCLC细胞生长并刺激SCLC细胞凋亡。SP类似物最初被表征为“广谱神经肽拮抗剂” 9。
作用方式
SP受体是一种G蛋白偶联受体,在许多方面与精神病学中其他经过充分研究的受体相似,特别是单胺受体2。SP与其受体的相互作用激活了Gq,Gq又激活了磷脂酶C,将磷脂酰肌醇双磷酸酯分解为肌醇三磷酸酯(IP3)和二酰基甘油(DAG)。IP3作用于肌质网中的特定受体以释放Ca2 +的细胞内储存,而DAG通过蛋白激酶C作用以打开质膜中的L型钙通道。细胞内[Ca2 +]的升高诱导组织反应。与SP所见的一系列动作一样,存在多种治疗可能性10。
功能
在中枢神经系统中,SP与情绪障碍,焦虑,压力,增强,神经发生,神经毒性和疼痛的调节有关。在消化道,SP,以及一些其他速激肽,是神经递质,调节运动活动,离子和液体的分泌,以及血管功能11,12。
参考
1. Argyropoulos SV, Nutt DJ (2000). Substance P antagonists: novel agents in the treatment of depression. Expert Opin Investig Drugs, 9(8):1871-1875.
2. Book: Substance P and Related Tachykinins. Chapter 13: Neuropsychopharmacology: By Nadia MJ, Kramer MS.
3. Senba E, Tohyama M (1985). Origin and fine structure of substance P-containing nerve terminals in the facial nucleus of the rat:an immunohistochemical study. Exp Brain Res., 57(3):537-546.
4. Seidel MF, Tsalik J, Vetter H, Müller W (2007). Substance P in Rheumatic Diseases. Current Rheumatology Reviews, 3:17-30.
5. Piercey MF, Dobry PJ, Einspahr FJ, Schroeder LA, Masiques N (1982) Use of substance P fragments to differentiate substance P receptors of different tissues. Regulatory Peptides, 3(5-6):337-349.
6. Shore SA, Drazen JM (1988). Airway responses to substance P and substance P fragments in the guinea pig. Pulm Pharmacol., 1(3):113-118.
7. Hanani M, Chorev M, Gilon C, Selinger Z (1988). The actions of receptor-selective substance P analogs on myenteric neurons: an electrophysiological investigation. European journal of pharmacology, 153(2-3):247-253.
8. Sakurada T, Yamada T, Tan-no K, Manome Y, Sakurada S, Kisara K, Ohba M (1991). Differential effects of substance P analogs on neurokinin 1 receptor agonists in the mouse spinal cord. J Pharmacol Exp Ther., 259:205-210
9. MacKinnon AC, Waters C, Jodrell D, Haslett C, Sethi T (2001). Bombesin and Substance P Analogues Differentially Regulate G-protein Coupling to the Bombesin Receptor. J. Biol. Chem., 276(30):28083-28091..
10. Khawaja AM, Rogers DF (1996). Tachykinins: receptor to effector. Int J Biochem Cell Biol., 28(7):721-738.
11. Leeman SE, Mroz EA (1974). Substance P. Life Sci., 15(12):2033–2044.
12. Wiesenfeld-Hallin Z, Xu XJ (1993). The differential roles of substance P and neurokinin A in spinal cord hyperexcitability and neurogenic inflammation. Regul Pept., 46(1-2):165-173





