《德国应用化学》VIP论文报道冯福德课题组在GSH−H2O2协同响应光敏剂的设计及其应用方面的研究进展
近期,我院冯福德课题组与中国科学院化学所王树研究员合作开发了一种GSH−H2O2协同响应的小分子光敏剂,并对其细胞内协同激活光动力治疗进行了应用研究。该成果以“GSH and H2O2 Co-Activatable Mitochondria-Targeted Photodynamic Therapy under Normoxia and Hypoxia”为题近期在线发表在德国应用化学杂志上(Angew. Chem. Int. Ed., 2020, DOI: 10.1002/anie.202003895),并被选为VIP论文。
基于肿瘤微环境设计可激活型的光敏剂(aPS)是近年来光动力治疗(PDT)研究领域的热点之一。多种内源性刺激因子协同参与光敏剂激活,在增强PDT过程的可控性和安全性方面具有重要应用价值。本研究根据还原型谷胱甘肽(GSH)和过氧化氢(H2O2)两种刺激因子在肿瘤细胞内的异常状态,设计了首个GSH−H2O2协同响应的线粒体靶向性aPS。如图1所示,mitoaPS含有苯并噻二唑母核结构,邻位硝基和烷硫基在特殊的GSH−H2O2氧化还原环境中经历自由基参与的一系列化学反应过程,激活双型(I型和II型)光动力反应,产生大量超氧负离子自由基和单线态氧等活性氧物种。mitoaPS具有很低的暗毒性,但在常氧、乏氧以及双光子激发等条件下都能产生显著的PDT功效。
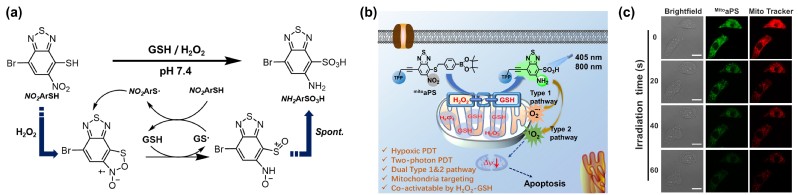
图1. (a)以NO2ArSH为分子原型的GSH−H2O2协同转化机制;(b)GSH−H2O2协同激活的PDT过程;(c)共聚焦显微镜下实时观察PDT效果。
巯基自由基参与的化学机制研究是在该课题组前期H2S−H2O2交互响应荧光探针(MRP,mutually responsive probe)研究工作基础上开展的(Chem. Eur. J.,2019, 25, 9164−9169)。这一类型探针荧光背景极低,在结合线粒体靶向性和跨键能量转移(TBET)响应机制的分子设计后,被用于探测含有H2S和H2O2的特殊氧化还原微环境(图2)。
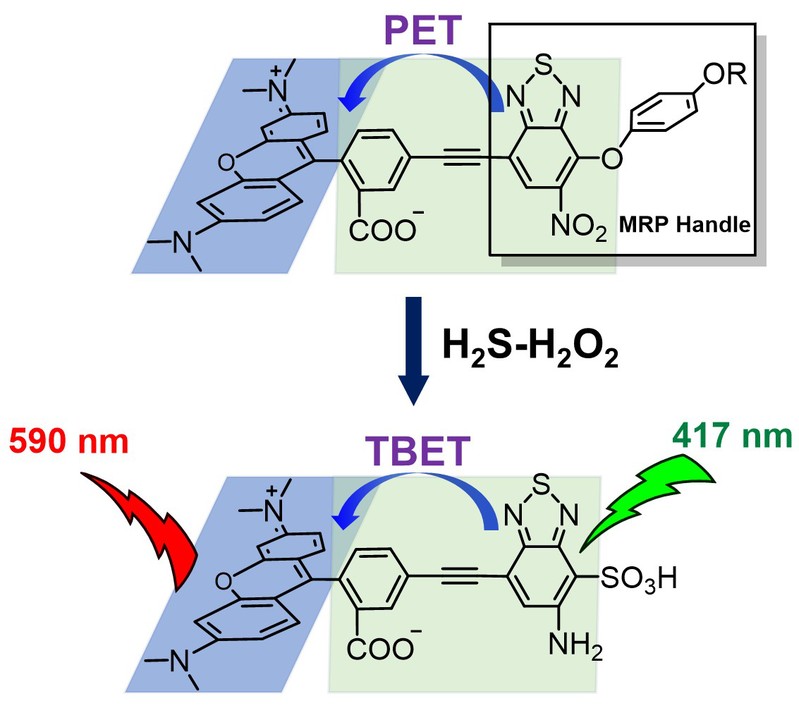
图2. H2S−H2O2参与的MRP把手片段自由基转化过程。
论文的第一作者为我院的助理研究员孙剑博士(南京大学化学化工学院2018年博士毕业生)。冯福德教授、王树研究员为该论文的共同通讯作者。南京大学郭子建院士、美国辛辛那提大学医学院刁佳杰教授给予了重要指导。该研究工作得到了国家重点研发计划等项目的资助。
版权与免责声明:本网页的内容由收集互联网上公开发布的信息整理获得。目的在于传递信息及分享,并不意味着赞同其观点或证实其真实性,也不构成其他建议。仅提供交流平台,不为其版权负责。如涉及侵权,请联系我们及时修改或删除。邮箱:sales@allpeptide.com