生科院贾永副教授与德国马普植物发育研究所联合在植物如何保持免疫“天平”两端“共栖微生物”与“病原微生物”的平衡方面取得重要进展
在自然土壤中生长的植物往往会被具有特定群落结构的微生物种群所定殖。当中包含了共栖微生物和病原微生物。在定殖过程中,植物经过长期进化形成一套复杂的先天免疫系统来保护自己。先天免疫系统一旦被共栖微生物或病原微生物相关分子模式(Microbe/Pathogen-associated molecular patterns, M/PAMP)激活,便会触发植物免疫反应( (MAMP)-triggered immunity, MTI),有效地限制病原微生物增殖。然而,如果植物免疫反应不加控制,不仅会抑制植物生长,同时会影响其它植物共栖微生物的定殖。那么,植物是如何在不影响对病原微生物的有效抗性前提下,实现共栖微生物的多样性定殖,仍然是未知的。

2021年5月24日,德国马克斯-普朗克植物育种研究所Paul Schulze-Lefert课题组和我校生科院贾永副教授联合在Nature Plants上发表了题为Coordination of microbe-host homeostasis by crosstalk with plant innate immunity的研究论文,自下而上的揭示了植物根部定殖的共栖微生物调节植物的免疫功能。这些共栖微生物间和植物间的微妙互动不但影响了宿主对病原微生物的抗性,也广义上协调共栖微生物与宿主植物免疫的动态平衡。
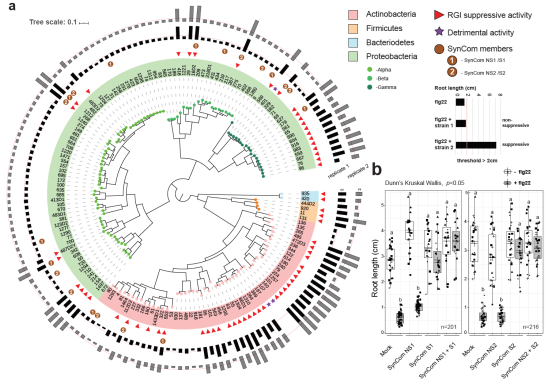
图1. 41%的拟南芥共栖微生物可缓解植物免疫激活下根部生长抑制。
论文研究结果显示41% (62/151)的拟南芥(Arabidopsis thaliana)根部细菌可以缓解通过M/PAMPs触发的拟南芥根部的生长抑制(Root growth inhibition, RGI)。作者继而通过对拟南芥根部合成细菌群落(synthetic communities/SynComs)的研究,确定了根部细菌可调节植物免疫反应(图1)。研究进一步发现,细菌群落在根部定殖时会改变174个与根系发育和养分运输密切相关的核心基因的表达。此外,對植物免疫反应有抑制性的SynComs可以特异性下调宿主植物免疫相关基因。作者透过(1)接种對植物免疫反应有抑制性的SynComs或(2)突变宿主植物共生时下调的转录因子MYB15,皆得出植物对机会性假单胞病原菌(Pseudomonasspp.)更加易感的结果。
不同的SynComs分别通过诱导或抑制MTI反应来调节宿主植物对病原微生物的易感性。因此,作者提出了一个变阻器模型(图2),在该模型中,植物允许多样的“微生物群落共栖”,主要是由于共栖微生物(具有MTI活性调节能力)相互作用可以缓冲植物免疫系统对病原微生物防御和免疫反应帶來生长抑制之间的矛盾,最终建立共栖微生物-寄主植物的体内稳态。

图2微生物群落共栖“变阻器模型”
综上所述,该研究首次探讨了植物是如何在不影响对病原微生物有效抗性的前提下,实现共栖微生物的多样性定殖,为植物免疫系统-共栖微生物-病原微生物三者关系的研究提供了新的方向与思路。
本文是以德国马克斯-普朗克植物育种研究所博士后Ka-Wai Ma、Yulong Niu和南京师范大学副教授贾永(Yong Jia)为本文的共同第一作者;德国马克斯-普朗克植物育种研究所Ruben Garrido-Oter和Paul Schulze-Lefert教授为本文共同通讯作者。本研究得到了国家留学基金、德国DFG基金的经费支持。
原文链接:https://www.nature.com/articles/s41477-021-00920-2
版权与免责声明:本网页的内容由收集互联网上公开发布的信息整理获得。目的在于传递信息及分享,并不意味着赞同其观点或证实其真实性,也不构成其他建议。仅提供交流平台,不为其版权负责。如涉及侵权,请联系我们及时修改或删除。邮箱:sales@allpeptide.com