凌飞教授课题组不用”分子”,而用”网络”预警结直肠癌中免疫逃逸相关的CD8+T细胞的耗竭
8月9日,华南理工大学凌飞教授课题组联合数学学院陈培博士后在Frontiers in Immunology(Q1; IF = 7.561)杂志发表了一篇题为Dynamic network biomarker of pre-exhausted CD8+ T cells contributed to T cell exhaustion in colorectal cancer的论文(论文链接:https://doi.org/10.3389/fimmu.2021.691142),凌飞教授为通讯作者及其2019级硕士研究生胡家麒为该文第一作者,韩重印等为署名作者,华南理工大学生物科学与工程学院为第一作者单位。

结直肠癌(colorectalcancer,CRC)全球范围内每年导致90万余人死亡。入院就诊的CRC患者大都已是III期或IV期的进展期患者。而IV期的患者5年存活率仅有10%左右。早发现早干预可提高患者生存率。近年来基于免疫检查点抑制剂(immune checkpoint inhibitors,ICI)的免疫疗法在多种恶性肿瘤治疗中取得突破性进展。最常见的免疫检查点PD-1/PD-L1通路的抑制剂,最近被证明是治疗少数晚期CRC的有效方法,但占绝大多数的晚期CRC患者采用ICI单药或不同ICI联合治疗却几乎无效。目前认为在恶性肿瘤发展的免疫逃逸阶段,肿瘤表面会过度表达免疫检查点分子,诱导CD8+T细胞耗竭,产生大量的耗竭性T细胞(Tex)。而PD-1通路阻断药物通常用于可能已经经历长期T细胞刺激的晚期癌症患者,此时可能大部分晚期CRC患者CD8+T细胞过度耗竭,已产生大量的Tex,PD-1抑制剂此时已无回天之术。我们认为,若能识别出预耗竭的CD8+T细胞亚群及其表面分子特征,鉴定出耗竭前发挥重要作用的关键网络分子(核心基因群),作为潜在的早干预靶点,以阻止产生更多的Tex而实现耗竭的逆转。与仅针对终末 Tex 细胞的治疗相比,靶向消耗殆尽前的 T 细胞可能具有更宽广的临床治疗窗口,最终使得免疫治疗药物在无效人群中获得进一步改善。
本研究采用动态网络生物标志物(DNB)的新方法,从系统生物学角度量化结直肠癌肿瘤组织中T细胞在调控网络中的免疫功能,从而预测T细胞耗竭前的关键时期,以进一步探究耗竭前T细胞在CRC免疫微环境中的作用,提供候选基因挖掘病人预后及免疫治疗相关靶点(Figure1)。
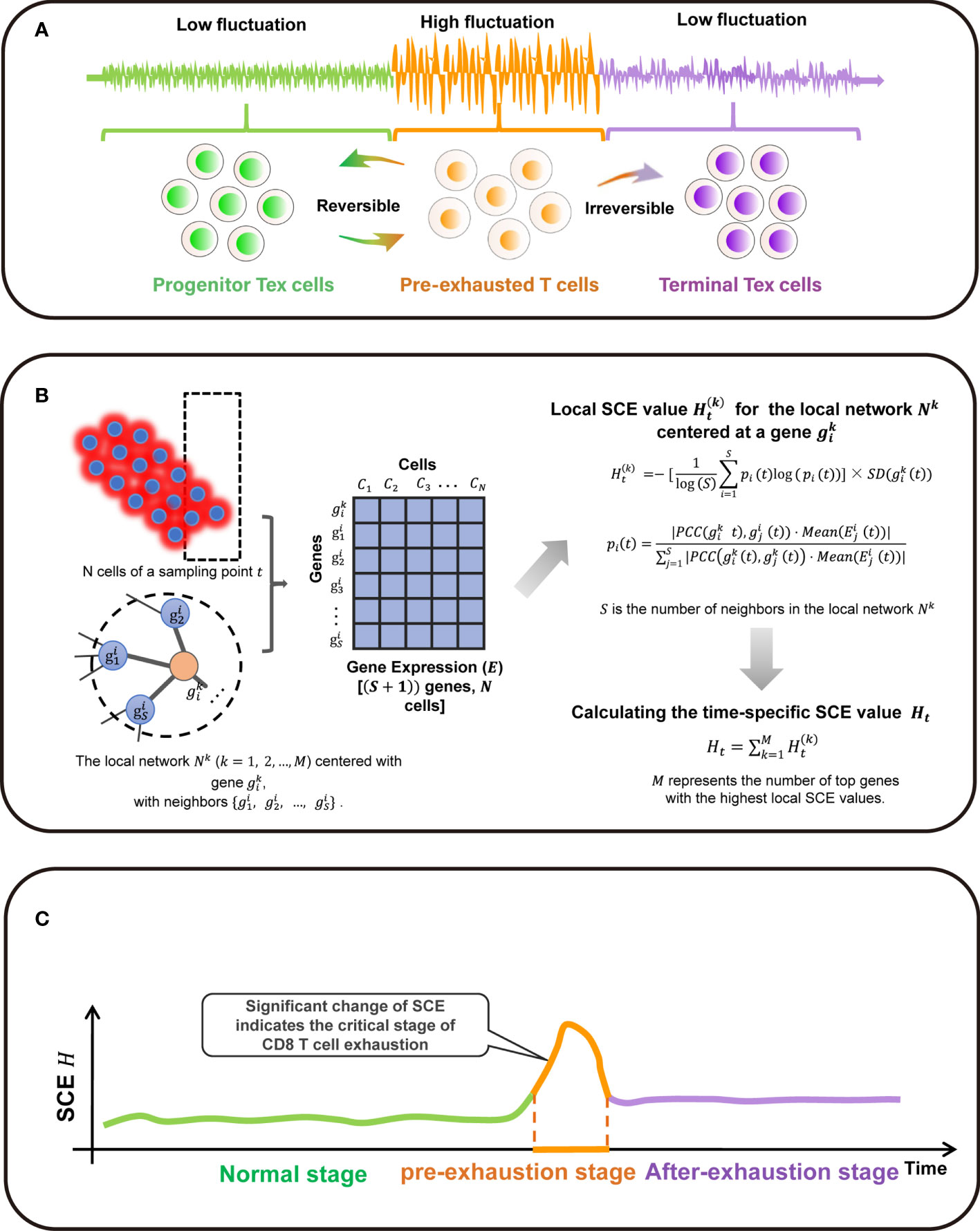
Figure1 动态网络标记物(DNB)算法构建
本研究为阐明 CRC 中 T 细胞耗竭的过程,利用scRNA-seq 数据构建了 CRC 肿瘤组织中的 CD8+ T 细胞耗竭性分化轨迹,并鉴定了耗竭前 T 细胞中的相关靶标和生物标志物(Figure2)。
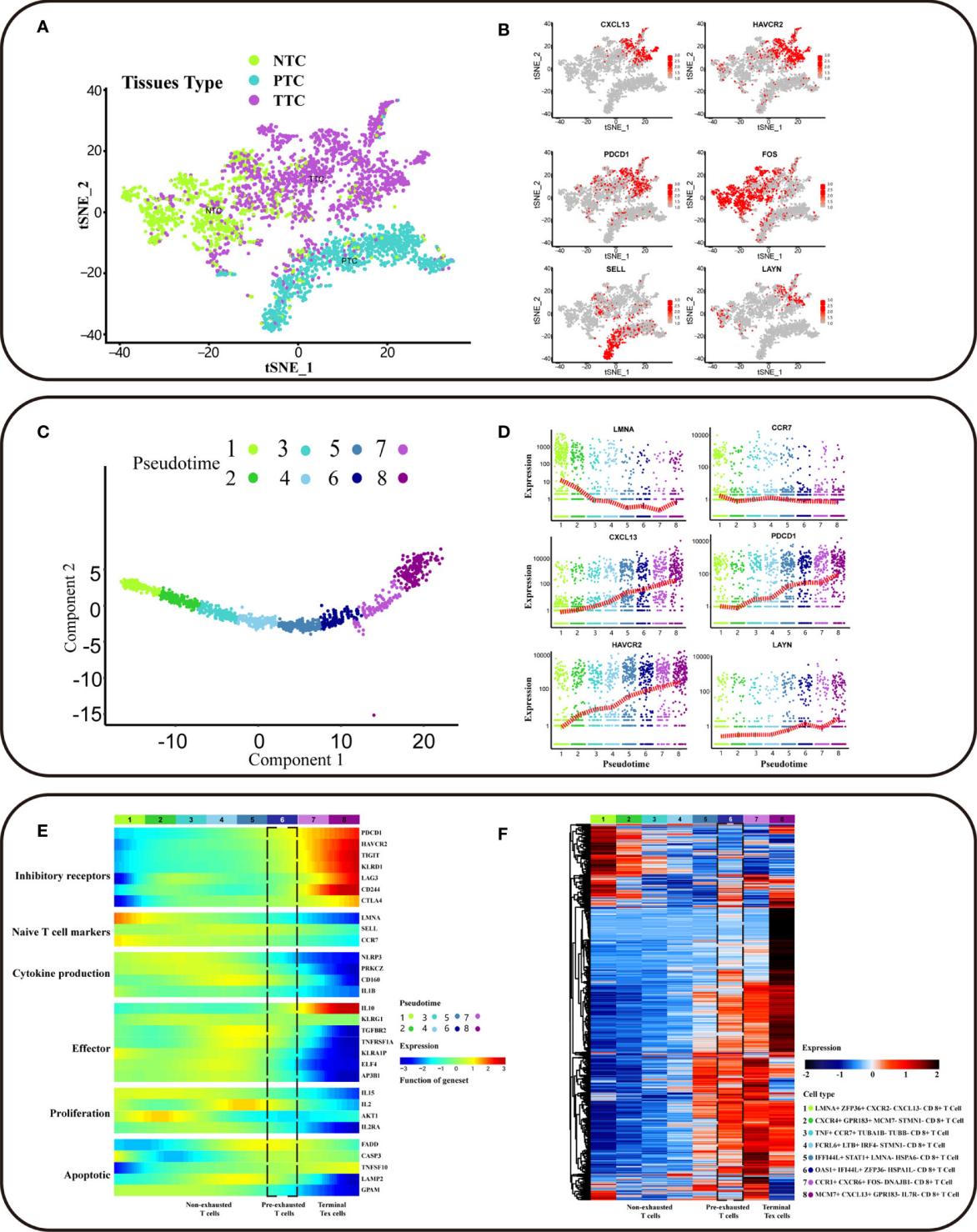
本研究还发现结直肠癌从II 期到 III 期的进展过程中,CRC 患者不同阶段的预耗竭 CD8+ T 细胞百分比增加,表明潜在的预耗竭 T 细胞分化方向与癌症进展相关(Figure3)。使用 TCGA 数据验证与耗竭前 T 细胞亚群相关的基因表达。CCT6A 作为DNB 基因网络表达的核心基因与 COAD 患者的总生存期显著相关(p = 0.026)。使用 DNB 方法鉴定的 DNB 核心基因 CCT6A 在DNB 核心基因网络中起着至关重要的作用。此外,CCT6A 还是与 CRC 预后相关的耗竭前 T 细胞亚群的生物标志物。

Figure3 CD8+ T 细胞亚型的鉴定和DNB核心基因生存分析
此外,本研究从 DNB基因和 DNB 相邻基因的网络中提取了DNB-neighboring DEG(差异表达基因) 和 DEGs 的子网络(Figure4)。这些与 DNB 相邻的 DEG 由 DNB 核心基因驱动。我们观察到 CCT 家族基因作为 DNB 核心基因驱动 TUBA1B 的翻转变化。我们发现 TUBA1B(目前癌症药物的治疗靶点之一)的表达与 DNB 基因 CCT6A 的表达同时增加。TUBA1B 是预耗竭 CD8+ T 细胞中 DNB 相邻的 DEG,与 CRC 患者的总生存期显着相关(p = 0.0082)。CCT6A 编码的蛋白质是分子伴侣,是包含 TCP1 复合物 (CCT) 的伴侣蛋白的成员,也称为 TCP1 环复合物 (TriC)。结合Reactome通路分析,我们推测CCT6A 驱动 TUBA1B表达,因为DEG 表达的协同增加可能导致 CD8+ T 细胞耗竭。
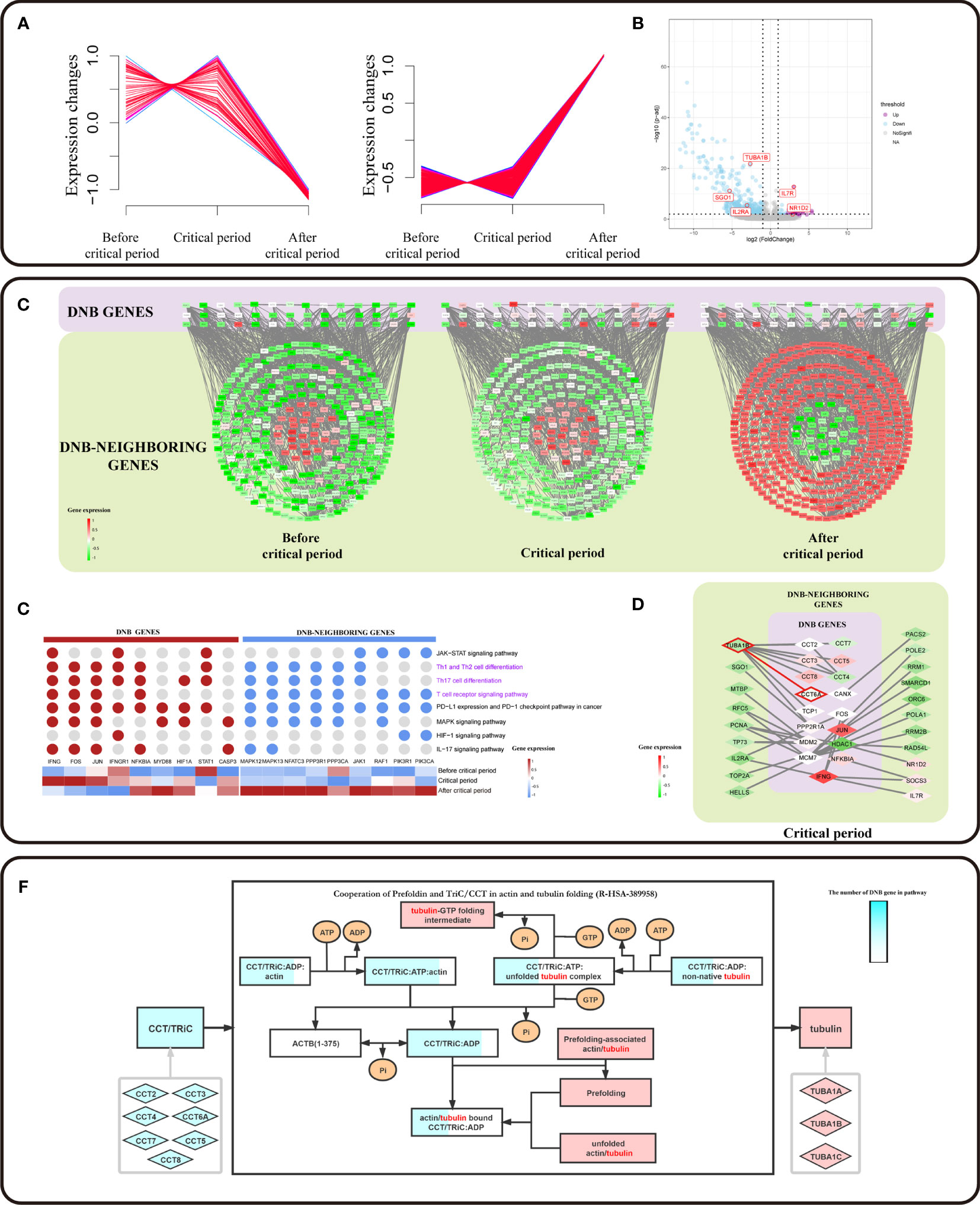
Figure4 DNB 核心基因驱动 DNB 相邻基因的翻转表达变化
本研究还探索了预耗尽的T 细胞和终末耗竭 T 细胞之间的细胞通讯,阐述了 Tex 细胞如何促进预耗竭T细胞的耗竭分化(Figure5)。总之,这项研究不仅成功地鉴定了结直肠癌免疫微环境中预耗竭的 T 细胞,而且还阐明了它们在网络和细胞水平上的 T 细胞耗尽中的双向作用。
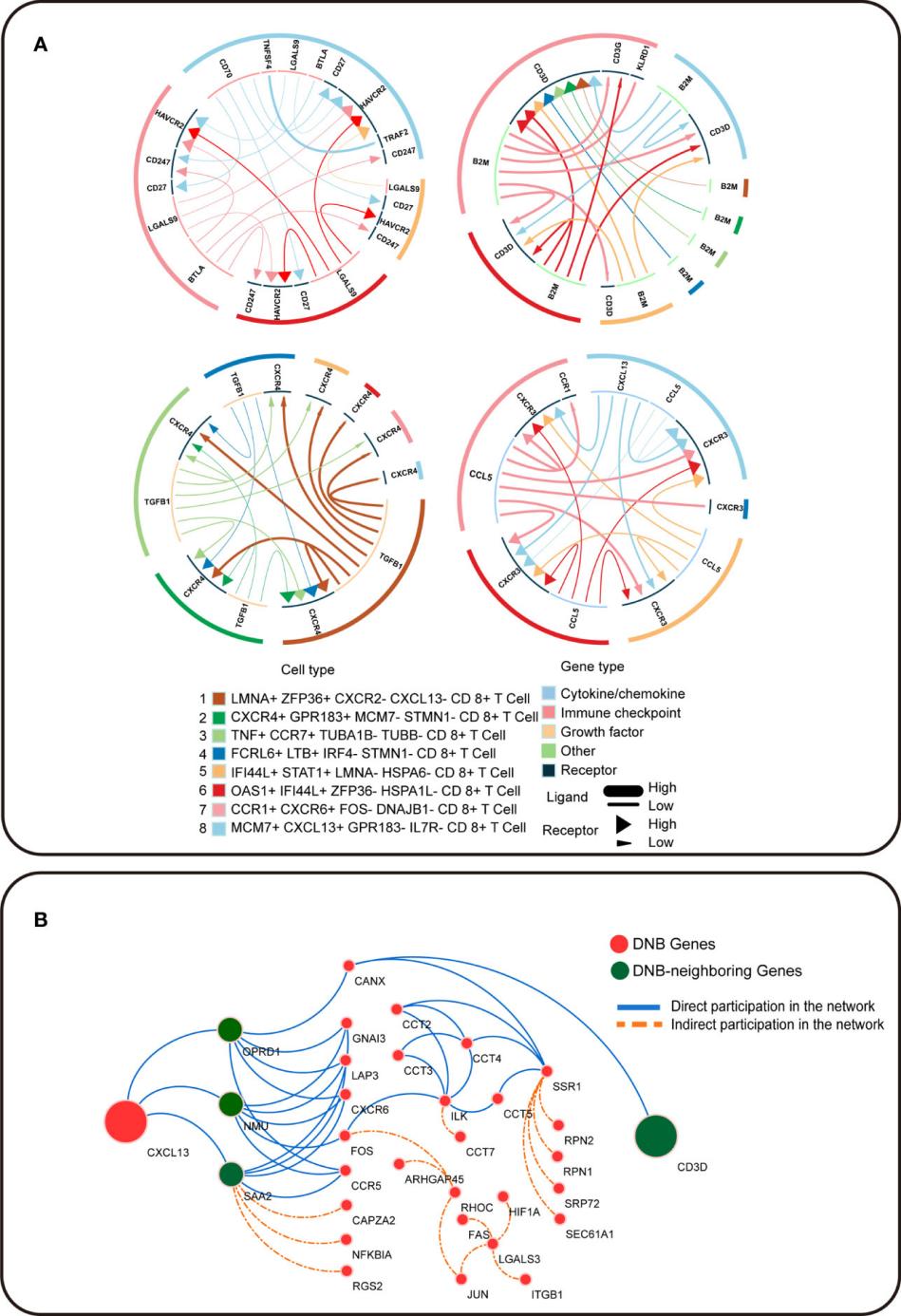
Figure5 T细胞耗竭中的细胞通讯
本研究整合了系统生物学、单细胞转录组学、免疫学等多学科研究,我们构建了CD8+ T 细胞发育轨迹,并使用动态网络生物标志物在单细胞水平鉴定了CRC 患者的预耗竭 T 细胞;同时,CCT6A 是耗竭前 T 细胞亚群的动态生物标志物。此外,TUBA1B 表达由 CCT6A 作为DNB 核心基因所驱动并导致 CD8+ T 细胞耗竭。值得注意的是,TUBA1B 和 CCT6A 表达均与结直肠癌患者的总生存期显著相关。本研究还观察到,终末耗竭 T 细胞和耗竭前 T 细胞之间的细胞通讯促使耗竭。这些发现提供了对 T 细胞耗竭机制的新见解,并为 CRC 的早诊断和早干预的靶向免疫治疗提供了新角度。
本研究得到了国家自然科学基金、广东省基础与应用基础研究基金的支持。
版权与免责声明:本网页的内容由收集互联网上公开发布的信息整理获得。目的在于传递信息及分享,并不意味着赞同其观点或证实其真实性,也不构成其他建议。仅提供交流平台,不为其版权负责。如涉及侵权,请联系我们及时修改或删除。邮箱:sales@allpeptide.com