北京大学分子医学研究所汪阳明研究组发现促进胚胎干细胞由原始态(naive)向始发态(primed)转化的微小RNA阅读次数:
2016年1月8日, 北京大学分子医学研究所汪阳明研究组在《Cell Research》杂志以Article长文在线发表题为“Pluripotency-associated miR-290/302 family of microRNAs promote the dismantling of naive pluripotency”的研究成果,首次报道了调控胚胎干细胞由原始态(naive)向始发态(primed)转化的微小RNA (microRNA,细胞中长度约22个碱基的非编码RNA,一般抑制基因表达) ,并解析了其作用机制,该研究对于胚胎干细胞在再生医学中的应用有重要意义。(http://www.nature.com/cr/journal/vaop/ncurrent/full/cr20162a.html)。
受精之后大约3到5天,尚未植入子宫(pre-implantation)的胚胎中生成了几十个原始态(naive)胚胎干细胞,这些细胞未来将分化成动物体内所有细胞。当胚胎植入子宫后(post-implantation),原始态干细胞很快迈出向特定细胞类型分化的第一步,变为始发态(primed)胚胎干细胞。利用具有不同化学成分的细胞培养液,科学家们可以从不同发育时期的小鼠胚胎中获取并永久培养原始态或始发态胚胎干细胞,但在人类和其它物种中则很难获取原始态胚胎干细胞。虽然原始态和始发态胚胎干细胞都具有分化成所有其他成体细胞的能力,但是始发态胚胎干细胞更难培养和进行基因操作,分化能力略低且不稳定, 因此原始态干细胞对于再生医学的应用价值更高。研究小鼠原始态到始发态胚胎干细胞的转化过程, 不仅可以揭示哺乳动物胚胎发育最早期细胞命运决定的秘密,而且对于再生医学有应用价值,可以帮助人们获得真正的人类原始态胚胎干细胞。
汪阳明研究组首先利用高通量测序分析了原始态和始发态干细胞中差异表达的微小RNA,发现在原始态到始发态转化的短暂过程(约2天)中上百个微小RNA的表达发生了显著变化, 暗示微小RNA可能参与了两种状态的转化。接着利用小RNA敲除的原始态干细胞,他们证实微小RNA对于原始态到始发态的转化不可或缺。最后通过筛选发现miR-290/302家族的微小RNA在这一转化过程中起主导作用,而其它多个微小RNA则起辅助作用。进一步的研究发现,miR-290/302家族通过抑制AKT通路以及促进ERK通路的活性帮助实现了原始态胚胎干细胞走出分化的第一步。本研究首次揭示了调控胚胎干细胞最早期分化的微小RNA及其作用机制,为在人类及其他物种中建立原始态多能干细胞提供了潜在的分子标志物和靶标。
北京大学分子医学研究所博士生顾凯丽,闫瑛,助理研究员张蔷和北京大学医学部副研究员李婷婷为共同第一作者。北京大学分子医学研究所博士生段菲菲和郝菁等也为本项目的完成做出了重要贡献。北京大学生命科学学院吴虹教授和前沿交叉学科研究院魏平教授提供了部分研究材料。该研究获得了北京大学-清华大学生命科学联合中心,科技部973计划及自然科学基金委创新群体和面上基金的支持。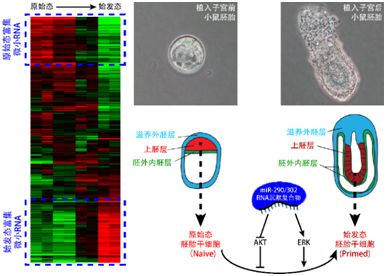
版权与免责声明:本网页的内容由收集互联网上公开发布的信息整理获得。目的在于传递信息及分享,并不意味着赞同其观点或证实其真实性,也不构成其他建议。仅提供交流平台,不为其版权负责。如涉及侵权,请联系我们及时修改或删除。邮箱:sales@allpeptide.com