摘要:
生物大分子在许多疾病的治疗中发挥着重要的作用, 但由于细胞膜的天然屏障作用, 只有分子质量小于600 Da 的分子才能穿透细胞膜进入细胞内。这使得一些有治疗价值但无细胞膜穿透性的分子在细胞生物学、药学等领域的应用受到极大的限制。近年来发现的一些具有细胞穿透功能的短肽 (少于 30 个氨基酸) 即细胞穿膜肽 (CPPs), 能够有效地将蛋白质、多肽、核酸片段等以多种方式导入多种哺乳动物细胞, 其转导效率高且不会造成细胞损伤。CPPs 的发现为生物大分子在细胞生物学、基因治疗、药物体内转运、临床药效评价以及细胞免疫学等研究领域等均具有良好的应用前景。本文就 CPPs 的种类特点、内化机制、应用及其存在的问题进行讨论和评述.
绝大多数疾病都需要在分子水平进行诊断治疗。而人们面临的一个主要问题是真核细胞和细胞器, 以及细胞壁和致病性微生物的膜, 使得许多具有很好的体外生物活性大分子包括药物不能进入细胞内, 以至于无法发挥其应有的作用。为克服这些生物活性大分子在体内转运的障碍, 人们已经发展了各种技术。运输遗传物质一般使用病毒载体, 但对于有些遗传病这种方法似乎不可行。非病毒的方法, 像电穿孔、显微注射及使用脂质体, 在常规和基因药物运输中得到了发展, 但显微注射法或电穿孔法对细胞具有创伤性, 可能损伤甚至破坏细胞膜, 属于侵袭性的方法。而非侵袭性的方法包括 pH 值敏感的脂质体, 要求在低酸环境下使膜失去稳定性从而释放药物进入胞浆, 对于人体生理环境中药物作用的研究具有一定局限性。
在过去的几十年里, 人们发现了一些肽和蛋白质能穿透细胞膜进入细胞内, 而且多种运载物分子也可以与这些肽和蛋白质连接并易位进入细胞内。这些肽和蛋白质载体构成一种新的很有潜力的药物运输载体,即细胞穿膜肽 (cell-penetrating peptides, CPPs), 它是一大类由 10~30 个氨基酸组成的短肽, 也称为蛋白质转导域 (protein translocation domain, PTD) 或“特洛伊木马”肽 (Trojan horse peptides) 或转导肽 (transduction peptide) 等。这些肽分子不会产生细胞膜永久性损伤, 并且毒性低。本文对于 CPPs的结构、性质、穿膜机制、应用前景及可能存在的问题等方面进行综述。
1 细胞穿膜肽的性质、分类及结构特征
到目前为止,已发现了多种 CPPs, 它们共有的性质[1]: ① 具有净正电荷性和两亲性; ② 穿膜转运效高; ③ 可以导入近乎所有的细胞; ④ 可以携带多种活性物质进入细胞; ⑤ 可以通过固相合成或原核表达制备, 方法成熟简便。CPPs 的分类以及统一的术语还没有。根据不同的分类标准, 得到不同的种类。最近有学者根据短肽的特点和来源将其分为 3 大类: ① 蛋白衍生肽(protein derived CPPs), 如 penetratin、TAT 和 pVEC等; ② 模型肽(model peptides) 如MAP和 (Arg) 7等; ③ 设计肽 (designed CPPs) 如 MPG 和Transportan等[2]。从其两亲性性质[3]也可将其分为 3 类: ① 两亲性 CPPs (PaCPPs), 如 MPG、transportan、TP10、Pep-1; ② 中等两亲性 CPPs (SaCPPs), 如 penetratin, RL16; ③ 非两亲性 CPPs (NaCPPs), 如 R9。
2 细胞穿膜肽的跨膜过程及其机制
有关 CPPs 的内化机制一直以来存在争议。不论通过何种机制穿膜, 理论上 CPPs 首先接近细胞膜的脂质层[4], 与其发生作用后进入细胞。
2.1 结合模式 目前认为 CPPs 与细胞膜的结合模式有两种[5], 多位点结合模式和静电吸引模式。多位点结合模式, 带正电荷的 CPPs 可能与细胞膜上带负电荷的葡糖胺聚糖结合, 也有可能与细胞膜上带负电荷的脂质结合。CPPs 中存在的带正电荷的碱性氨基酸与细胞膜上带负电荷的物质结合是 CPPs 穿膜的必要条件。静电吸引模式, 即通过疏水性吸附作用, 靠近膜表面的肽段发生非特异性的静电积聚。Ziegler 等[3]根据 CPPs 的两亲性程度分别阐述了其与膜的结合机制以及其在膜上的定位。PaCPPs 与膜结合时主要靠疏水作用插入膜内, 结构发生改变(α 螺旋或 β 折叠结构的形成), 且不耗能。SaCPPs 在与膜结合时结构发生改变, 通过静电作用轻微插入脂质双分子层。相反, NaCPPs 与膜结合时仅仅轻微吸附于膜上, 不会插入到脂质分子层中。PaCPPs 与SaCPPs 在穿膜时都会使脂质层发生紊乱, 形成跨膜静电域,一些 CPPs 自组装会进一步扰乱脂质双分子层的完整性。而在低摩尔浓度、低阴离子脂质组分膜条件下, SaCPPs、NaCPPs 与膜之间不会发生相互作用。关于易位过程中肽与膜之间作用后形成的结构, 人们也提出了很多种模型[6]: 反相胶束模型, 局部电穿孔, 暂时的孔结构[7, 8], 诱导膜融合, 内吞通道[9]或几种模型的结合。
2.2 内化机制 关于 CPPs 的内化机制 (穿膜机制/易位机制/转导机制) 一般可分为两种[10, 11]: 转导(易位) 模式, 包括直接穿膜和跨膜转导模式, 跨膜转导模式 (translocation models)[12]又包括反转微团(inverse micells)、地毯 (carpet) 及打孔 (barrel stave) 模型 (图 1); 内吞模式 (endocytosis), 包括网格蛋白(clathrin, 120 nm)、脂质筏/小窝蛋白(caveolin, 50~80 nm)[13, 14]和巨胞饮 (macropinocytosis, 1~5 μm) 介导的模式 (图 2)。转导模式与内吞模式的主要不同在于转导的 CPPs 在穿膜后直接定位于细胞质, 而内吞的CPPs 被限制在囊泡中。一般来说, 当 CPPs 运载小的亲水性药物时, 多肽诱导膜紊乱使肽直接易位进入胞内; 而当运载大的亲水性药物时膜紊乱程度较低, 内吞作用似乎是比较合适的易位机制[11]。
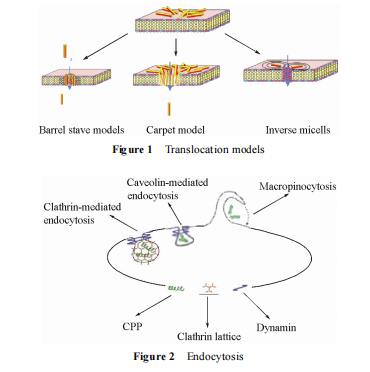
巨胞饮介导的内吞作用[15]是最近提出的一种CPPs 运载大分子药物 (MW > 30 000 Da) 的入胞机制, 它是一种非网格蛋白、非脂质筏介导的依赖肌动蛋白的一种非特异性内吞过程。最近的研究重点是巨胞饮作用并认为其是细胞内化的主要途径, 它能在不同程度上发生于所有的细胞内, 而且可以从膜的边缘扰动和形成囊泡的大小两个方面区分巨胞饮与其他形式的内吞作用。
最近, 人们又提出了一种有关富含胍盐基团的CPPs 的单独运输或其与小分子 (MW < 3 000 Da) 结合的运输机制。CPPs 的胍盐基团可以与细胞表面的负电性基团形成二齿状的氢键, 产生的离子对在膜电位的作用下易位穿过细胞膜, 离子对在膜内部分离, 释放出 CPPs 到细胞质中。也有可能是不同平衡离子 (两亲性的或亲水性的) 的存在将导致 CPPs 的电荷中和或电荷重置, 这类 CPPs 在物理性质上的动力学因素的改变将促使其分配进入脂质双分子层中(穿膜过程)。也有研究[16]认为阳离子穿膜肽与磷脂离子配对克服了穿膜过程中存在的固有能垒, 以一种非内吞作用的形式进入细胞内。不过, 研究证明, 一些外源两亲性平衡离子, 如十二烷基硫酸钠或磷脂酰甘油/无机磷酸盐在非生理条件下加入能够促进CPPs 的体内内化。
CPPs 介导的无论小分子还是大分子的细胞内运输机制有多种。一般来说, CPPs 或 CPP 与小分子的结合物内化进入细胞是通过静电作用和形成氢键的易位或转导作用; 而 CPP 与大分子的结合物是通过能量依赖的内吞作用, 特别是巨胞饮作用内化进入细胞[17]。含有胍盐基团的 CPPs 可能以一种平衡离子介导的特殊穿膜机制进入细胞内。然而, 在这几种情况下, CPPs 与细胞表面的阴性残基的直接接触是成功穿膜的必要条件。
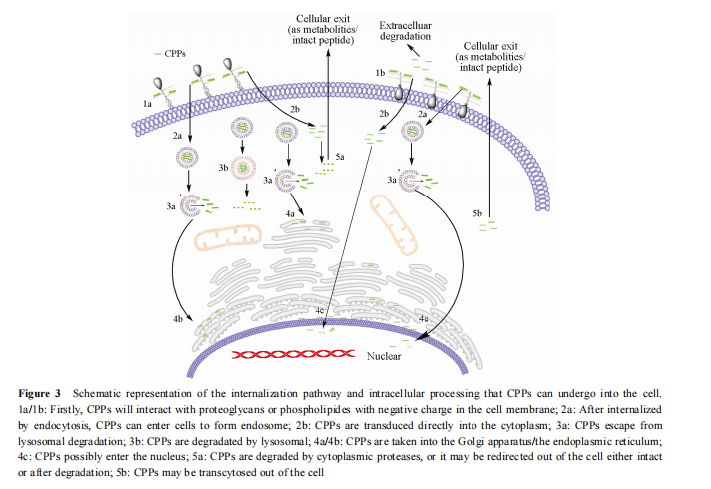
CPPs 与药物分子或基因或颗粒结合内化后的历程与药物分子、基因或颗粒本身的性质、CPPs 的性质及所选用的细胞体系密切相关。CPPs 或 CPPs-药物分子可能的内化历程[10]如图 3 所示。如果 CPPs 或CPPs-药物分子直接易位进入细胞质中, 可能会与细胞质中的一些靶向物相互作用, 使 CPPs 或 CPPs-药物分子被运输到核内、被细胞质中的蛋白酶降解或很可能以完整分子或降解后的分子形式转运到细胞外; 如果 CPPs 或 CPPs-药物分子是以内吞作用机制内化, 其历程取决于内吞机制的类型, CPPs 或 CPPs-药物分子很可能经过溶酶体降解、可能在降解前从胞内体(内涵体) 中逃逸出来随后进入细胞质中, 有可能进入核内, 到达高尔基体或内质网中或胞吞转运到细胞外。
2.3 不同性质的 CPPs 的内化机制 不同性质的CPPs 会有不同的内化通道[3]。在低摩尔浓度和低阴离子脂质组分膜条件下, 只有 PaCPPs 在通过脂质双分子层时呈现出直接易位作用, 且它们的直接易位作用在大分子药物[18]和荧光基团的存在下减少。相反, SaCPPs 的直接易位作用要求在较高的肽浓度(>100 μmol·L−1) 和较高的阴离子脂质组分膜的条件下才能发生。NaCPPs 则要求更高的肽浓度 (>1 mmol·L−1) 和阴离子脂质组分膜 (70%) 才能够扰乱膜发生直接易位作用。即在低摩尔浓度下, 内吞作用具有优势, 而直接易位作用在高浓度下才可能发生。
2.4 影响 CPPs 内化机制的因素 在评估细胞穿膜肽的内化有效性过程中存在不一致现象的原因是由于在比较时忽略了所用载体、药物分子、浓度和细胞类型, 药物分子的物理化学性质, 如亲水性和所带电荷可能会影响内化作用, 特别是非内吞作用的内化机制[19]。Patel 等[10]也提出在衡量 CPPs 内化作用时存在多方面的挑战。因此, 非常有必要找出影响 CPPs内化机制的因素。
肽分子的性质与细胞膜的组成部分何者是主要的影响因素, 跨膜电位与肽/细胞比率何者更重要[20]?目前的研究表明, 肽与细胞表面蛋白聚糖之间相互作用和跨膜电位的存在都至关重要[12]。研究[21]发现, CPPs 与药物的结合降低了内化的有效性, 并极大地改变了 CPPs 的细胞内分布。也有研究认为小分子的药物不影响内化的效率, 但大分子药物, 内化效率明显降低[2]。还有学者认为, 不同的穿膜肽在携带不同分子时采取的进胞方式可能有差异, 同时其进胞时间也会不同[11]。
从 CPPs 本身的结构性质来看, 肽分子的共同性质两亲性以及净正电荷对肽分子与膜和药物分子之间发生相互作用非常重要[6]。肽的结构和对肽的构象[22]有影响的环境因素都会对内化能力产生重要影响。肽结构的多样性, 可能与它的两亲性或它的净正电荷一样是细胞自内化和其与脂质的相互作用所必需的特性。如果肽必须溶解在不同的环境中像水和膜中, 它就必须通过调节构象[23]来适应外部的环境。
综合来看, 影响 CPPs 内化机制的因素主要有: 温度、肽浓度、细胞周期、药物分子大小及其理化性质、非固定化细胞中不同的亚细胞分布类型、CPPs的理化性质 (氨基酸构成、分子大小、分子构象)、所用的细胞系、胞内体中肽的降解、早期肽从胞内体中的逃速度及所结合配体的荧光强度等。
3 细胞穿膜肽的应用
大量研究表明, 穿膜肽具有强大的运载潜能, 与其他生物大分子转运方式相比,穿膜肽的转导作用具有许多独特之处[24]。CPPs 携带的物质可以为蛋白质(绿色荧光蛋白、RNA 酶、半乳糖苷酶等)、多肽 (100个氨基酸残基以下[23])、DNA、化学小分子药物、寡核苷酸 (100 bp 以下[23])、反义核酸、肽核酸、纳米颗粒、荧光素、有机分子、腺病毒载体、成像物质、脂质体及铁颗粒等。运载能力[1]可以达到 120 kDa (如半乳糖苷酶)、40 nm (如铁颗粒), 没有明显的证据表明运载极限。细胞穿膜肽可以通过化学结合或基因融合等方式携带各种生物大分子[5]。CPPs 与药物的连接方式有两种: 非共价连接和共价连接。通过使用CPPs 还可以增加肽类药物的活性, 以及进行细胞器官的特异性运输[25]。近年 CPPs 的应用进展如下。
3.1 蛋白质及多肽类药物的运输 对许多疾病使用外源蛋白质或多肽类药物是一个非常有价值的治疗方法。Wu 等[26]利用穿膜肽的蛋白转导功能来介导信号肽-绿色荧光蛋白-穿膜肽 NT4-GFP-Ant 融合蛋白通过细胞膜和血脑屏障到达靶细胞。Tat (Tat48−60) 能将细胞周期蛋白依赖激酶抑制剂的细胞毒素肽模拟物 P21EAF1/CIP1运输到细胞核内, 且研究[27]发现Tat48−60–P10 可以诱导细胞凋亡。Zhang 等[28]根据一种 α 螺旋肽 CAI 的结构设计出了一种细胞穿膜肽NYAD-1, 它比 CAI 具有更稳定的 α 螺旋结构, 研究发, NYAD-1能够穿过细胞膜并与Gag聚蛋白共定位于质膜上, 破坏病毒颗粒的自组装。研究者[29]设计了一种含有穿膜肽、弹性蛋白类似多肽 ELP (Val-Pro-Gly-Xaa-Gly) 和一种衍生于细胞周期蛋白依赖激酶抑制剂 P21 的结合多肽, 这种多肽能够使 SKOV-3 卵巢癌细胞和HeLa 子宫癌细胞的生长速率减慢而抑制它们的增殖。HIV-Tat 与小泰勒虫抗原 Tp2 结合形成重组at-Tp2 融合蛋白, 发现其能够加强迟钝的 CD8+T 细胞反应的兴奋性[30]。
3.2 核酸类药物的运输 核酸类药物的细胞运输具有挑战性。最近有关使用 CPPs 进行核酸细胞运输的例子较多。研究证明, 细胞膜穿透性寡肽——八聚精氨酸(R8) 修饰的脂质体可以有效输送 siRNA 进入细胞并增强其生物学功能[31]。PalmApergi 等[32]研究一种细胞穿膜肽 MAP, 用这种典型的抗菌肽处理细菌产生细菌空壳, 这种空壳可以载入所需的 DNA 或质粒并将其运输进入哺乳动物细胞内, 还可以用于预防接种。Meade 等[33]研究认为, CPPs 为双链 siRNA 进行细胞内化去诱导 RNAi 反应提供了一种好方法。Veldhoen 等[34]研究发现一种新的载体肽 MPGα 能同时与核酸形成非共价连接的、具有高灵活性的复合物, 它可以作为运输 siRNA 的载体。
与转座子结合的“睡美人”转座酶能将特殊基因转移进目标动物体内。这些特殊基因有助于治疗多种疾病。有研究[35]发现细胞穿膜肽 M918 可以完成“睡美人”转座酶和一个外源转座子质粒 (带有一种抗生素基因) 在体外的细胞内共转导运输。具有空间位阻的带电荷中性寡核苷酸类似物, 如 肽 核 酸 (PNA) 和 磷酰 二 胺 吗啉代寡 核 苷 酸(PMO), 在反义引物的应用方面具有很好的生物学和药理学性质。然而, 寡聚核酸在细胞内不能自由运输, 因此, Lebleu 等[36]研究了两种富含精氨酸的 CPPs (R-Ahx-R)4AhxB (R= 精氨酸, Ahx = 胺己苯酸酯, B= β-丙氨酸) 和 R6Pen, 它们能够在胞内体溶解剂存在的情况下, 在低摩尔浓度下将 PNA 和 PMO 进行有效的核运输。研究发现, 固相合成穿膜肽 Tat 能够携带质粒 DNA 穿过细胞膜进行基因转染, 并对细胞活性无明显影响[37]。
3.3 颗粒运输 Liu 等[38]将 Tat 分子连接到生物活性聚合物核/壳纳米粒的表面形成 Tat-PEG (聚乙醇)- b-chol (胆固醇) 复合物。研究发现, 其可以穿过血脑屏障 (BBB) 进行药物运输, 并可以进入神经元细胞质。Wei 等[39]研究发现使用一种异型双功能偶联剂硫代琥珀酰亚氨基-4-对马来酰亚氨基苯基丁酸酯 (sulfosuccinimidyl-4-(p-maleimidophenyl)-butyrate, SSMPB) 将 HIV-1 Tat 与 MS2 (噬菌体衣壳) VLPs (病毒样颗粒) 结合, 此颗粒可以抑制丙型肝炎病毒(HCV) 的 5'-非翻译区 (VTR) 和内核糖体进入位点(IREs) 的反义 RNA 的翻译。Lu 等[40]研究发现, 结核分歧杆菌膜蛋白 McelA 可以与胶态金颗粒和乳胶微球结合在 HeLa 细胞内内化。生物纳米颗粒 BNC 是一种含有乙型肝炎病毒表面抗原 L-蛋白的空心纳米粒。BNC 只能运输基因或药物进入特定的人类肝细胞中, 因此 Shishido 等[41]试图从遗传学上通过引入CPPs 的方法改变 BNC 的特异性。结果表明, CPPs 与BNC 的结合能够在短时间内有效的内化进入各种细胞系, 而且没有明显的细胞毒性。
3.4 小分子药物运输 研究表明, 富含精氨酸的细胞穿膜肽可以直接运输磷酸二酰胺吗啉齐聚物进入鼠类白细胞, 抑制其基因表达和改变前体 mRNA 的剪接[42]。Lindgren 等[43]设计了一种 CPP 与细胞抑制剂甲氨蝶呤 (MTX) 的结合物, 用于克服乳腺癌肿瘤细胞对甲氨蝶呤的耐受。将 2', 5'-寡腺甙酸四聚物(2-5A) 与短链 HIV-1Tat 肽用化学方法结合产生2-5A-Tat 嵌合体[44], 此嵌合体可以被细胞吸收并能在完整的细胞中活化核糖核酸酶 L, 它可能为 HIV的RNA 在体内的靶向破坏提供了一种方法。
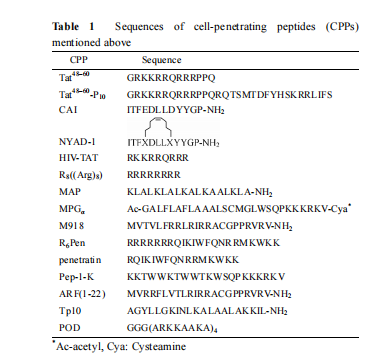
3.5 增强药物的吸收及其他特殊功能 Kamei 等[45]发现通过使用 CPPs 可以促进胰岛素的肠内吸收。Khafagy 等[46]研究发现 L-型穿膜肽 penetratin 可以显著增加胰岛素的渗透性而使其穿过鼻膜, 并对鼻吸收黏膜上的细胞完整性不会引起明显的破坏。Tunnemann 等[47]研究认为细胞穿膜肽介导的肽转导作用不仅是一种对细胞内 Ca2+无副作用情况下可以增加心肌功能的唯一方法, 而且是一般细胞或干细胞中蛋白质之间相互作用的调节和控制的非常有用的工具。Kloss 等[48]研究发现, 含有 4~10 个精氨酸残基的寡聚精氨酸, 特别是 (Arg)8 能够抑制细胞内主要的蛋白水解系统。当考虑寡聚精氨酸作为药物的细胞内运输载体时, 必须考虑其对蛋白酶的抑制活性问题。有研究报道, 成功设计的一种新的穿膜肽Pep-1-K (衍生于穿膜肽Pep-1) 具有强的抗菌活性, 可以作细菌选择性抗菌肽[49]。Johansson 等[50]研究发现了一种含有 22 个氨基酸残基的衍生于肿瘤抑制基因 P14ARF 的 N 端部分的肽 ARF (1-22), 它是一种具有 P14ARF 功能的类似物, 对细胞膜有穿透性, 膜破坏性低且能诱导细胞凋亡。以前研究认为大多数CPPs 可以易位穿过哺乳动物细胞质膜, 而不能穿过像酵母细胞的细胞膜。然而, Parenteau 等[51]对 20 种CPPs 进行了测试, 发现有一种肽 Tp10 能有效的穿过裂殖酵母细胞并在细胞内均匀分布。由于治疗分子不能穿过质膜, 基因和药物运输进入眼部组织, 例如视网膜和角膜被阻碍, Johnson 等[52]研究发现了一种能用于眼部组织运输的新肽 POD, 能够运输小分子和大分子药物进入神经视网膜上皮细胞和角膜细胞等。如果能够通过高分辨率成像技术追踪干细胞的分布和分化的能力, 对临床和研究非常重要。Liu等[53]用一种典型的 CPP 承载钆颗粒, 此颗粒可以用于骨髓间质干细胞的磁共振成像。荧光成像技术确定此复合物可以内化进入干细胞质和核内,毒性实验和流式细胞仪分析表示此复合物不会影响细胞的生存和膜电势梯度。关于 CPPs 的氨基酸序列见表 1。
4 细胞穿膜肽在应用中存在的问题
CPPs 在治疗应用中存在的主要问题是使药物分子到达细胞质去诱导所需的生物反应, 药物分子必须从胞内体中逃逸出来。胞内体的释放是各种阳离子CPPs 细胞内运输过程中的主要限速步骤, 有报道称可以使用胞内体-瓦解肽、酸敏感的腙键或激光触发胞内体孔使胞内体释放等。Shiraishi 等[54]提出光化学内化 (PCI) 方法, 通过使用光敏剂可以有效地释放嵌入胞内体中的药物分子。但这些物质的应用对其他方面是否有影响目前尚不清楚。因此, 有关胞内体的释放还需要进一步研究。一旦 CPPs 承载药物分子进入细胞内, 另一个面临的问题是怎样把药物分子运输到生物活性位点。可以通过将肽序列与细胞内信号序列结合解决。但此法是否可行还有待探究。将穿膜肽用作临床药物的运输工具, 首先必须确认肽本身不会对正常细胞造成不利影响, 由于CPPs 具有高阳离子性[55], 因此人们担心它们会和其他的阳离子多聚物如聚 L-赖氨酸或聚乙烯亚胺 (PEI) 一样存在一定的毒性。一般来说, CPPs 在高浓度肽下才会产生细胞毒性, 但两亲性强的 PaCPPs 在低摩尔浓度下已经具有细胞毒性[3]。在这方面已进行了一些研究, 但大多是体外实验[11]。
CPPs 与治疗性分子的结合物几乎分布于身体的各个部分而不依赖于给药的方式。基于 CPPs 缺乏细胞特异性的性质, 人们试图通过将带有负载的 CPPs与细胞特异识别分子相结合介导特异性细胞运输。与所设想一致, 细胞特异抗体与 CPPs 的结合确实增加了它们的细胞内化作用。它也同时明显地减少了抗体在体内的选择性。研究表明, 抗体的应用不易满足靶向性要求。目前, 抗体的直接靶向性所面临的主要问题: 肽分子进入细胞的非特异性与抗体和其靶向细胞的特异性配体的亲和性之间存在一定的冲突。因此, 有研究者认为将 CPPs 的穿膜活性暂时隐蔽起来, 直到 CPPs-抗体复合物到达靶向组织和适合的细胞周围后再使 CPPs 释放[56]。另有学者设想, 通过对药物靶向组织所分泌的蛋白酶敏感的化学键将 CPPs 与某种药物分子相连[57], 从而使得靶向药物分子聚集在靶标组织周围。
CPPs 在药物运输过程中的使用存在的另外一个弊端是其稳定性差。CPPs 内化后, 由于体内含有各种蛋白酶, 它可能会酶解外源 CPPs 及其药物分子; 体内的环境包括 pH 值、离子浓度等都有可能改变CPPs 的某些性质使其失去活性。因此, 必须通过寻找新的稳定的CPPs[58]或对现有的 CPPs 进行修饰改进来解决这方面的问题。一些蛋白在内化进入细胞后不再具有生物活性, 可以考虑在蛋白和 CPPs 之间插入一个连接分子来辅助在细胞内释放有活性的蛋白和药物。此外, CPPs 是否有免疫原性或半免疫原性及长期应用会对机体产生何种影响, 需要将 CPPs 序列进一步的优化以提高其适用性[59]。一些证据显示, CPPs可以与任意的分子结合, 非靶向性进入细胞内, 导致生物活性药物不必要的损失。因此, 如果不能建立可行性使用方法以促进细胞特异性运输, 将限制细胞穿膜肽在机体内运输药物等方面的应用。
目前, 在能够有效利用 CPPs 运输药物以充分发挥治疗作用方面有价值的应用实验结果还鲜见报道。这种载药方式在应用中是否存在潜在的细胞毒性以及运输过程中缺乏细胞特异性等问题尚未引起足够的的重视[60]。一些 CPPs 存在细胞内化差, 出现细胞内代谢性降解及一些不良的生物效应如毒性和免疫原性等。需要进一步开展对 CPPs 的药代动力学、体内分布等相关研究。
5 展望
CPPs 的发现为生物大分子用于疾病治疗带来了曙光, 在细胞生物学、基因治疗、药物体内转运、评价及细胞免疫学等研究领域均具有良好的应用前景。但在 CPPs 真正应用于临床前仍有一系列问题需要解决。CPPs 在体内缺乏组织特异性和细胞类型特异性, 因此增加转导肽的靶向性则是将来发展的一个目标, 需要构建靶向部分。而噬菌体展示技术筛选出来的细胞特异 CPPs 提供了一个很有前景的方法。因 CPPs在体内的酶解性, 体内运输效果的不确定性, 可能存在的神经毒性和免疫原性等, 最近细胞穿膜非肽分子载体得到发展, 如肌醇、蔗糖、乳糖、多羟糖醇 (山梨醇) 等[61]。除了 CPPs 外, 一些含有几个氨基酸 (从3到10个) 具有细胞特异性并且可以通过内吞作用内化的不同肽相继被发现, 这些肽称为细胞靶向肽(CTPs)[55], 并用于各种治疗分析中。CTPs 与一些给定的细胞系专有表达的受体之间的相互作用具有高特异性和很强的亲和性。鉴于 CPPs 表现出的穿膜特性与 CTPs 表现出的高特异性和亲和性。CPPs 与CTPs 的共用是否能达到希望的运输目的, 还需要进一步研究。





