生物素-(Arg8)-加压素是一种经过巧妙设计的肽类激素,作为加压素受体的激动剂,表现出无与伦比的选择性,特别是针对备受尊敬的V1A和V1B亚型。
编号:192680
CAS号:126703-17-1
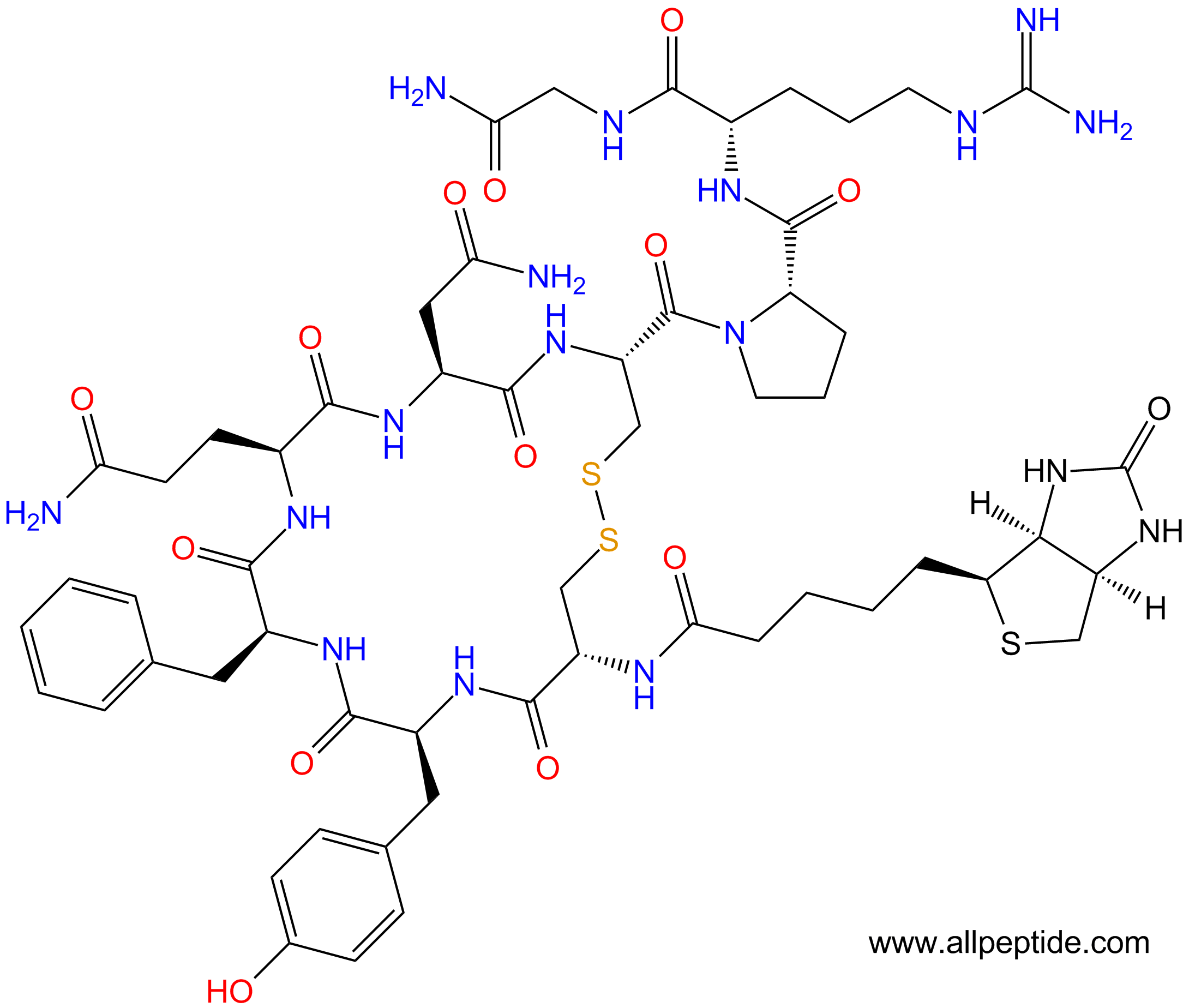
单字母:Biotinyl-CYFQNCPRG-NH2(Disulfide Bridge:C1-C6)
| 编号: | 192680 |
| 中文名称: | 生物素标记的抗利尿激素:Biotin-精氨加压素、Biotin-[Arg8] Vasopressin /AVP |
| 英文名: | Biotin-[Arg8] Vasopressin /AVP |
| 英文同义词: | Biotinyl-(Arg8)-Vasopressin |
| CAS号: | 126703-17-1 |
| 单字母: | Biotinyl-CYFQNCPRG-NH2(Disulfide Bridge:C1-C6) |
| 三字母: | Biotinyl-Cys-Tyr-Phe-Gln-Asn-Cys-Pro-Arg-Gly-NH2(Disulfide Bridge:Cys1-Cys6) |
| 氨基酸个数: | 9 |
| 分子式: | C56H79N17O14S3 |
| 平均分子量: | 1310.53 |
| 精确分子量: | 1309.52 |
| 等电点(PI): | - |
| pH=7.0时的净电荷数: | 3.94 |
| 平均亲水性: | -0.64285714285714 |
| 疏水性值: | -0.73 |
| 消光系数: | 1490 |
| 来源: | 人工化学合成,仅限科学研究使用,不得用于人体。 |
| 盐体系: | 可选TFA、HAc、HCl或其它 |
| 储存条件: | 负80℃至负20℃ |
| 标签: | 生物素标记肽(Biotinyl) 二硫键环肽 激动剂多肽(Agonist Peptide) 抗利尿激素 |
生物素-(Arg8)-加压素是一种经过巧妙设计的肽类激素,作为加压素受体的激动剂,表现出无与伦比的选择性,特别是针对备受尊敬的V1A和V1B亚型。
Biotinyl-(Arg8)-Vasopressin is an ingeniously engineered peptide hormone exhibiting unparalleled selectivity as an agonist for vasopressin receptors, particularly targeting the esteemed V1A and V1B subtypes.
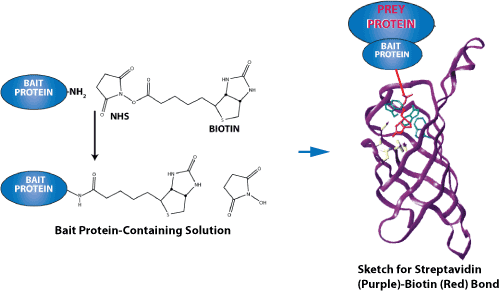
专肽生物合成用于蛋白质-蛋白质相互作用研究的生物素化肽。尽管生物素可以在 N 端或 C 端引入(通过赖氨酸残基),但我们建议使用 N 端修饰,因为它成本低、成功率高、周转时间短且易于操作。因为多肽合成是从 C 端到 N 端合成的,因此,N 端修饰是 SPPS步骤的最后一步,不需要额外的特定缩合步骤。相比之下,C 端修饰需要额外的步骤,并且通常更复杂。当然,原则上生物素可以定位在任何地方。

生物素可以通过多种不同的接头或间隔物与肽分离。尽管如此,还是建议包含一个灵活的间隔物,例如 Ahx(一个 6 碳接头),以使生物素标签更加稳定或灵活。
专肽生物在 N 端或 C 端提供生物素化:生物素-N 端、赖氨酸-生物素-肽中间和赖氨酸-生物素-C 端。
专肽生物还可以使用 Ahx 接头或长碳 (LC) 接头提供生物素化:生物素-Ahx-N 末端、Lys-Ahx-生物素-肽中间、Lys-Ahx-生物素-C-末端。
(生物素结构)
示例:
GRGDS在N端和C端标记生物素的结构展示。
1、GRGDS在N端标记生物素,不增加Ahx 接头
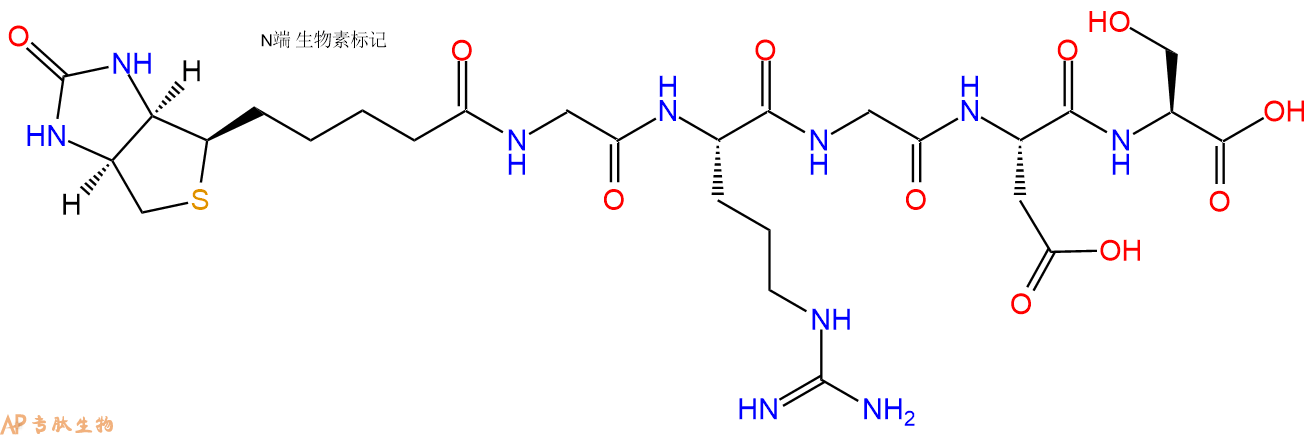
2、GRGDS在N端标记生物素,增加一个Ahx 接头

3、GRGDS在C端标记生物素,不增加Ahx 接头
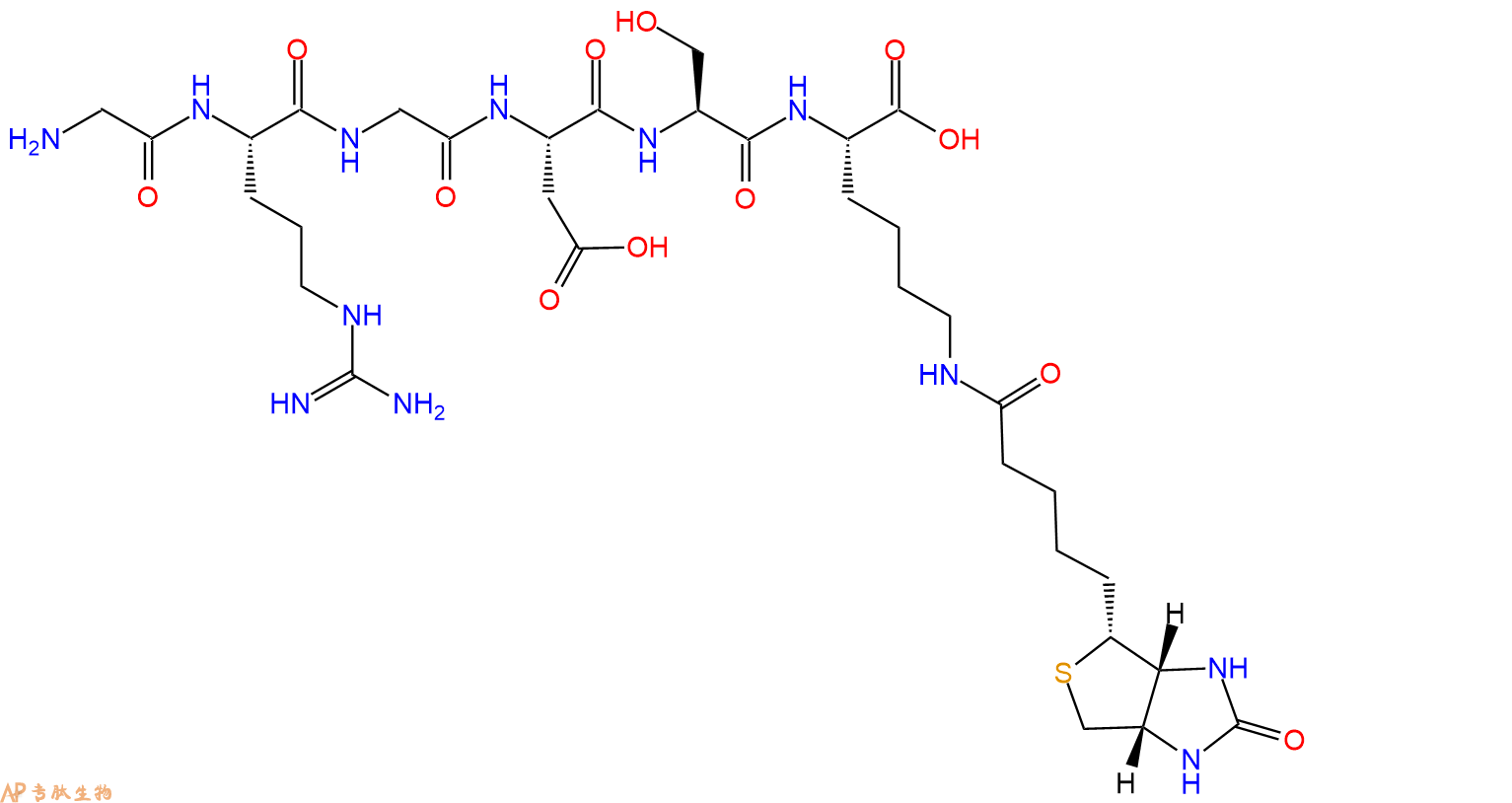
4、GRGDS在C端标记生物素,增加一个Ahx 接头。
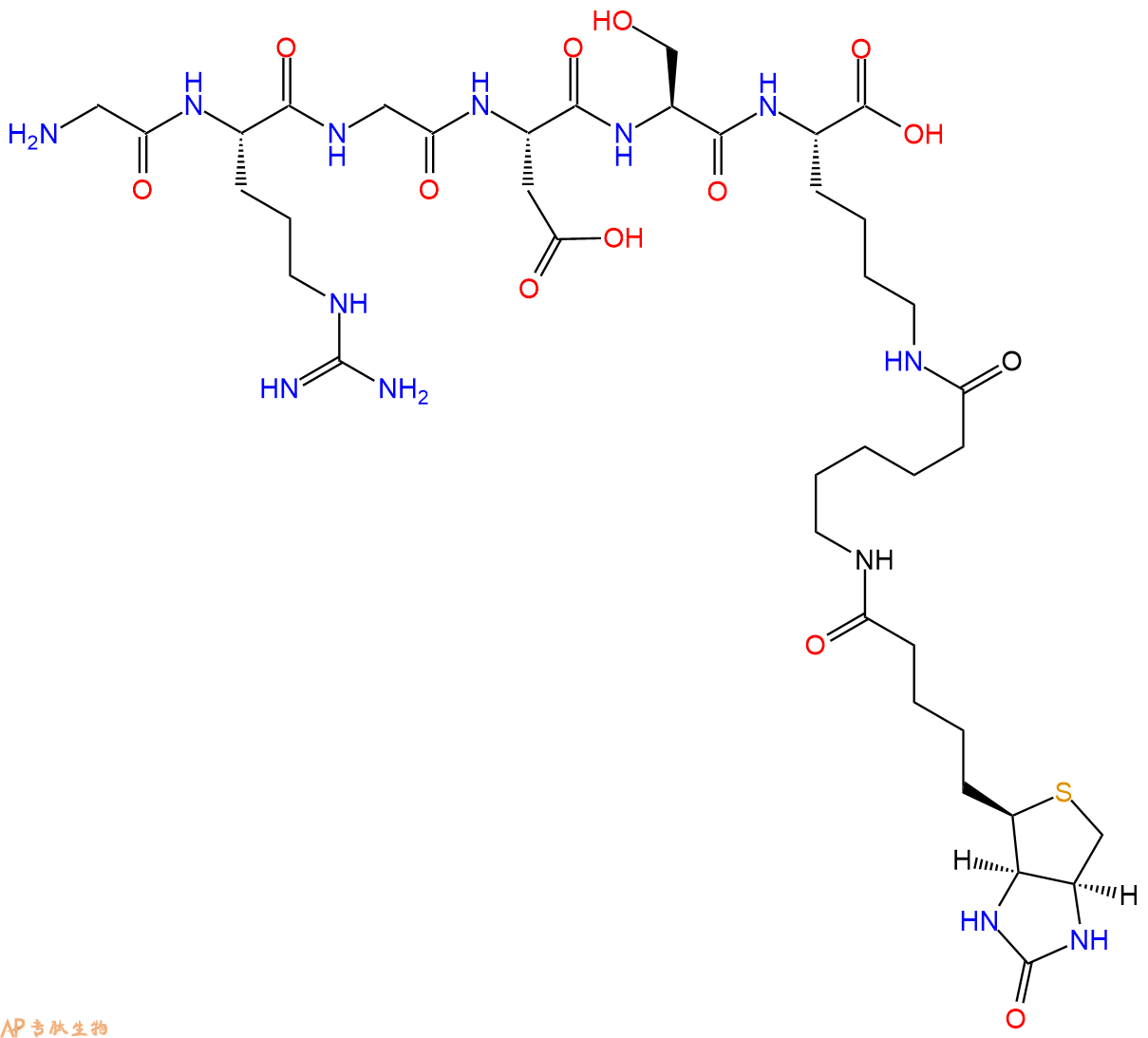
二硫键广泛存在与蛋白结构中,对稳定蛋白结构具有非常重要的意义,二硫键一般是通过序列中的2个Cys的巯基,经氧化形成。
形成二硫键的方法很多:空气氧化法,DMSO氧化法,过氧化氢氧化法等。
二硫键的合成过程, 可以通过Ellman检测以及HPLC检测方法对其反应进程进行监测。
如果多肽中只含有1对Cys,那二硫键的形成是简单的。多肽经固相或液相合成,然后在pH8-9的溶液中进行氧化。
当需要形成2对或2对以上的二硫键时,合成过程则相对复杂。尽管二硫键的形成通常是在合成方案的最后阶段完成,但有时引入预先形成的二硫化物是有利于连合或延长肽链的。通常采用的巯基保护基有trt, Acm, Mmt, tBu, Bzl, Mob, Tmob等多种基团。我们分别列出两种以2-Cl树脂和Rink树脂为载体合成的多肽上多对二硫键形成路线:
二硫键反应条件选择
二硫键即为蛋白质或多肽分子中两个不同位点Cys的巯基(-SH)被氧化形成的S-S共价键。 一条肽链上不同位置的氨基酸之间形成的二硫键,可以将肽链折叠成特定的空间结构。多肽分 子通常分子量较大,空间结构复杂,结构中形成二硫键时要求两个半胱氨酸在空间距离上接近。 此外,多肽结构中还原态的巯基化学性质活泼,容易发生其他的副反应,而且肽链上其他侧链 也可能会发生一系列修饰,因此,肽链进行修饰所选取的氧化剂和氧化条件是反应的关键因素, 反应机理也比较复杂,既可能是自由基反应,也可能是离子反应。
反应条件有多种选择,比如空气氧化,DMSO氧化等温和的氧化过程,也可以采用H2O2,I2, 汞盐等激烈的反应条件。
空气氧化法: 空气氧化法形成二硫键是多肽合成中最经典的方法,通常是将巯基处于还原态的多肽溶于水中,在近中性或弱碱性条件下(PH值6.5-10),反应24小时以上。为了降低分子之间二硫键形成的可能,该方法通常需要在低浓度条件下进行。
碘氧化法:将多肽溶于25%的甲醇水溶液或30%的醋酸水溶液中,逐滴滴加10-15mol/L的碘进行氧化,反应15-40min。当肽链中含有对碘比较敏感的Tyr、Trp、Met和His的残基时,氧化条件要控制的更精确,氧化完后,立即加入维生素C或硫代硫酸钠除去过量的碘。 当序列中有两对或多对二硫键需要成环时,通常有两种情况:
自然随机成环: 序列中的Cys之间随机成环,与一对二硫键成环条件相似;
定点成环: 定点成环即序列中的Cys按照设计要求形成二硫键,反应过程相对复杂。在 固相合成多肽之前,需要提前设计几对二硫键形成的顺序和方法路线,选择不同的侧链 巯基保护基,利用其性质差异,分步氧化形成两对或多对二硫键。 通常采用的巯基保护 基有trt, Acm, Mmt, tBu, Bzl, Mob, Tmob等多种基团。





